Tham khảo Bài 12 (Liên kết cộng hoá trị), hãy:
a) Mô tả sự hình thành liên kết trong phân tử halogen bằng công thức electron.
b) Liên kết trong phân tử halogen là liên kết cộng hoá trị phân cực hay không phân cực?
c) Dựa vào bán kính nguyên tử (Hình 6.2), hãy dự đoán xu hướng biến đổi độ dài liên kết trong dãy các phân tử halogen.
Tham khảo Bài 12 (Liên kết cộng hoá trị), hãy:
a) Mô tả sự hình thành liên kết trong phân tử halogen bằng công thức electron.
b) Liên kết trong phân tử halogen là liên kết cộng hoá trị phân cực hay không phân cực?
c) Dựa vào bán kính nguyên tử (Hình 6.2), hãy dự đoán xu hướng biến đổi độ dài liên kết trong dãy các phân tử halogen.
Câu hỏi trong đề: Bài tập Nhóm halogen có đáp án !!
Quảng cáo
Trả lời:
a) Phân tử halogen: Mỗi nguyên tử halogen có 7 electron hoá trị, hai nguyên tử halogen liên kết với nhau bằng cách mỗi nguyên tử halogen góp 1 electron, tạo thành một cặp electron dùng chung. Khi đó, trong phân tử X2 (X: halogen), mỗi nguyên tử đều có 8 electron ở lớp ngoài cùng, thoả mãn quy tắc octet:
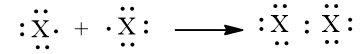
b) Liên kết trong phân tử halogen là liên kết cộng hoá trị không phân cực.
c) Bán kính tăng dần từ F < Cl < Br < I và độ âm điện giảm dần từ F > Cl > Br > I.
⇒ Dự đoán: độ dài liên kết X – X (X: halogen) tăng dần từ F2 đến I2.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đổi 80 000m3 = 80 000 000 L = 8.107 L
5 mg Cl2 được dùng để khử trùng 1 L nước sinh hoạt.
x mg Cl2 được dùng để khử trùng 8.107 L nước sinh hoạt.
⇒ x = mg = 400 kg
Lời giải
- Số oxi hóa của chlorine trong Cl2 là 0.
- Số oxi hóa của chlorine trong HCl là -1.
- Số oxi hóa của chlorine trong HClO là +1.
- Số oxi hóa của chlorine trong HClO2 là +3.
- Số oxi hóa của chlorine trong HClO3 là +5.
- Số oxi hóa của chlorine trong HClO4 là +7.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.