Câu hỏi trong đề: Bài tập Liên kết hóa học có đáp án !!
Quảng cáo
Trả lời:
Đáp án:
Trả lời:
Đáp án đúng là: C
Bước 1: Tổng số electron hóa trị trong phân tử = 1.5 + 2.6 = 17 electron
Bước 2: Trong phân tử NO2, nguyên tử N cần 3 electron để đạt octet, nguyên tử O cần 2 electron hóa trị để đạt octet. Vì vậy, N là nguyên tử trung tâm, còn các nguyên tử O được xếp xung quanh: O – N – O
Bước 3: Mỗi nguyên tử O cần 6 electron hóa trị để đạt octet:
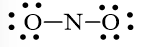
Bước 4: Số electron hóa trị còn lại là 17 – 6.2 – 2.2 = 1
Mà nguyên tử N chưa đạt octet nên 1 nguyên tử O sẽ dùng 1 cặp electron hóa trị để tạo liên kết với nguyên tử N và trên nguyên tử N vẫn còn 1 electron chưa tham gia liên kết.
Công thức Lewis của NO2 là
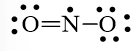 hoặc
hoặc 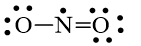
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Trả lời:
Mô hình VSEPR được sử dụng để mô tả dạng hình học của các phân tử dựa trên lực đẩy giữa các cặp electron hóa trị. Để sử dụng mô hình VSEPR, công thức phân tử của chất được viết dưới dạng AXnEm. Trong đó:
A: nguyên tử trung tâm;
X: nguyên tử liên kết với nguyên tử A; n là số nguyên tử;
E: cặp electron hóa trị chưa liên kết của nguyên tử A; m là số cặp electron;
Lưu ý: Nếu nguyên tử trung tâm lẻ một electron thì electron đó vẫn được tính tương đương một cặp electron.
+ Trường hợp AXn (với n = 2, 3, 4, …)
• Với n = 2, phân tử có cấu trúc thẳng.
• Với n = 3, phân tử có cấu trúc tam giác phẳng.
• Với n = 4, phân tử có cấu trúc tứ diện.
+ Trường hợp AXnEm
• Với dạng AX2E, phân tử có dạng góc.
• Với dạng AX3E, phân tử có dạng tháp tam giác.
• Với dạng AX2E2, phân tử có dạng góc.
Có một số trường hợp mô hình VSEPR không giải thích được hình dạng phân tử nhưng có thể giải thích theo sự lai hóa orbital nguyên tử như CH4, NF3, …
Có 3 trạng thái lai hóa cơ bản: lai hóa sp3, lai hóa sp2 và lai hóa sp.Lời giải
Trả lời:
a) Phân tử BeH2.
Cấu hình electron hóa trị của Be: 2s2.
Trong nguyên tử Be, một AO 2s tổ hợp với 1 AO 2p, tạo ra hai AO lai hóa sp.
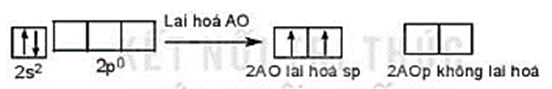
Hai AO lai hóa sp của nguyên tử Be xen phủ với hai AO s của hai nguyên tử H tạo thành hai liên kết σ giữa Be – H.
b) Phân tử SO2.
Cấu hình electron hóa trị của S: 3s23p4.
Trong nguyên tử S, một AO 3s lai hóa với hai AO p, tạo ra ba AO lai hóa sp2.
S còn AO p chứa 1 electron độc thân sẽ xen phủ 1 AO p chứa 1 electron độc thân của O hình thành liên kết π và AO chưa lai hóa có 1 electron độc thân sẽ tiếp tục xen phủ với OA p của nguyên tử O đó để hình thành liên kết σ. Với nguyên tử O còn lại thì nguyên tử S dùng AO chứa 2 electron để xen phủ với 2 AO chứa electron độc thân của nguyên tử O còn lại.
c) Phân tử NH3.
Cấu hình electron hóa trị của N: 2s22p3.
Trong nguyên tử N, 1 AO 2s và 3 AO 2p của nguyên tử N lai hóa với nhau tạo nên 4 AO lai hóa sp3 giống hệt nhau, hướng về 4 đỉnh của hình tứ diện đều. Trên 3 AO lai hóa có electron độc thân. Trên AO lai hóa còn lại có cặp electron ghép đôi.
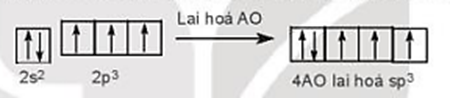
Ba AO lai hóa chứa electron độc thân của nguyên tử N xen phủ với 3 AO 1s chứa electron độc thân của 3 nguyên tử H, tạo nên 3 liên kết σ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















