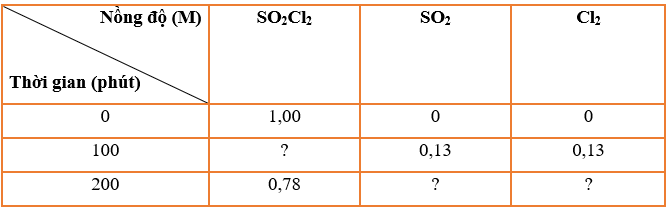
Cho phản ứng:
2N2O5(g) → 4NO2(g) + O2(g)
Sau thời gian từ giây 61 đến giây 120, nồng độ NO2 tăng từ 0,30 M lên 0,40 M. Tính tốc độ trung bình của phản ứng.
Cho phản ứng:
2N2O5(g) → 4NO2(g) + O2(g)
Sau thời gian từ giây 61 đến giây 120, nồng độ NO2 tăng từ 0,30 M lên 0,40 M. Tính tốc độ trung bình của phản ứng.
Quảng cáo
Trả lời:
Tốc độ trung bình của phản ứng là:
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
a) Biểu thức tốc độ tức thời của phản ứng:
b) - nồng độ O2 tăng 3 lần, nồng độ NO không đổi
⇒ Tốc độ phản ứng tăng 3 lần
- nồng độ NO tăng 3 lần, nồng độ O2 không đổi
⇒ Tốc độ phản ứng tăng 9 lần
- nồng độ NO và O2 đều tăng 3 lần
⇒ Tốc độ phản ứng tăng 27 lần.
Lời giải
H2(g) + Cl2(g) → 2HCl(g)
a) Biểu thức tốc độ tức thời của phản ứng viết theo định luật là:
b) Nồng độ H2 giảm 2 lần và giữ nguyên nồng độ Cl2
⇒
Vậy tốc độ phản ứng giảm một nửa khi nồng độ H2 giảm 2 lần và giữ nguyên nồng độ Cl2
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.