Dữ liệu thí nghiệm của phản ứng:
SO2Cl2(g) → SO2(g) + Cl2(g) được trình bày ở bảng sau
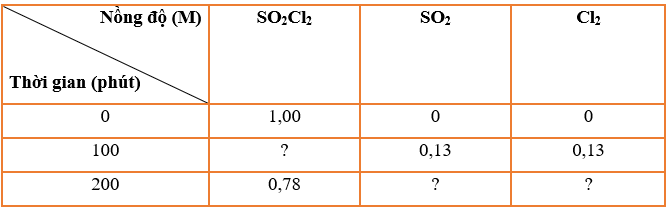
a) Tính tốc độ trung bình của phản ứng theo SO2Cl2 trong thời gian 100 phút.
b) Sau 100 phút, nồng độ của SO2Cl2 còn lại là bao nhiêu?
c) Sau 200 phút, nồng độ của SO2 và Cl2 thu được là bao nhiêu?
Dữ liệu thí nghiệm của phản ứng:
SO2Cl2(g) → SO2(g) + Cl2(g) được trình bày ở bảng sau

a) Tính tốc độ trung bình của phản ứng theo SO2Cl2 trong thời gian 100 phút.
b) Sau 100 phút, nồng độ của SO2Cl2 còn lại là bao nhiêu?
c) Sau 200 phút, nồng độ của SO2 và Cl2 thu được là bao nhiêu?
Quảng cáo
Trả lời:
a) Tốc độ trung bình của phản ứng theo SO2Cl2 trong thời gian 100 phút.
(M/phút)
b) Sau 100 phút, nồng độ của SO2Cl2 còn lại là 1,00 – 0,13 = 0,87 M
c) Sau 200 phút, nồng độ của SO2Cl2 còn lại là: 0,78 M
⇒ Nồng độ của SO2Cl2 đã phản ứng là: 1,00 – 0,78 = 0,22 M
⇒ nồng độ của SO2 và Cl2 thu được là 0,22 M
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
a) Biểu thức tốc độ tức thời của phản ứng:
b) - nồng độ O2 tăng 3 lần, nồng độ NO không đổi
⇒ Tốc độ phản ứng tăng 3 lần
- nồng độ NO tăng 3 lần, nồng độ O2 không đổi
⇒ Tốc độ phản ứng tăng 9 lần
- nồng độ NO và O2 đều tăng 3 lần
⇒ Tốc độ phản ứng tăng 27 lần.
Lời giải
H2(g) + Cl2(g) → 2HCl(g)
a) Biểu thức tốc độ tức thời của phản ứng viết theo định luật là:
b) Nồng độ H2 giảm 2 lần và giữ nguyên nồng độ Cl2
⇒
Vậy tốc độ phản ứng giảm một nửa khi nồng độ H2 giảm 2 lần và giữ nguyên nồng độ Cl2
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















