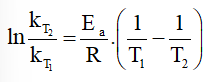Vận dụng khái niệm năng lượng hoạt hoá để giải thích vai trò của xúc tác trong một số quá trình tự nhiên như: tiêu hoá thức ăn trong cơ thể người, động vật, ... và một số quá trình sản xuất: sulfuric acid, acetic acid, rượu, bia, ...
Vận dụng khái niệm năng lượng hoạt hoá để giải thích vai trò của xúc tác trong một số quá trình tự nhiên như: tiêu hoá thức ăn trong cơ thể người, động vật, ... và một số quá trình sản xuất: sulfuric acid, acetic acid, rượu, bia, ...
Câu hỏi trong đề: Bài tập Năng lượng hoạt hóa của phản ứng hóa học có đáp án !!
Quảng cáo
Trả lời:
Trả lời:
Năng lượng hoạt hóa (Ea) là năng lượng tối thiểu mà các chất phản ứng cần có để phản ứng hóa học có thể xảy ra. Để phản ứng hóa học xảy ra thì các phân tử chất phản ứng phải va chạm vào nhau, nhưng không phải va chạm nào đều gây ra phản ứng, mà chỉ những va chạm có hiệu quả mới gây ra phản ứng. Trên thực tế có rất nhiều phản ứng có năng lượng hoạt hóa lớn như: tiêu hoá thức ăn trong cơ thể người, động vật, ... và một số quá trình sản xuất: sulfuric acid, acetic acid, rượu, bia, ...
⇒ Chất xúc tác làm phản ứng theo nhiều giai đoạn, mỗi giai đoạn có năng lượng hoạt hóa thấp hơn năng lượng của phản ứng khi không có xúc tác, do đó làm tăng tốc độ phản ứng.
Ví dụ:
- Có ba loại enzyme tiêu hóa chính. Chúng được phân loại dựa trên các phản ứng mà chúng giúp xúc tác:
1. Amylase phân hủy tinh bột và carbohydrate thành đường.
2. Protease phân hủy protein thành các axit amin.
3. Lipase phân hủy lipid, là chất béo và dầu, thành glycerol và axit béo.
- Platinium (Pt), vanadium pentoxide (V2O5) được sử dụng trong quá trình oxi hóa SO2 thành SO3 để sản xuất sulfuric acid.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Trả lời:
Khi nhiệt độ tăng từ 300 K lên 310 K thì tốc độ phản ứng tăng 3 lần.
⇒
Mà ⇒
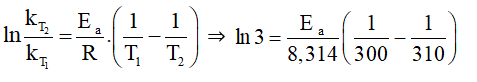
⇒ Ea = 84 944,92 J/mol ≈ 85 kJ/mol
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.