Cho hằng số tốc độ của một phản ứng là 11M-1.s-1 tại nhiệt độ 345 K và hằng số thực nghiệm Arrhenius là 20 M-1.s-1 . Tính năng lượng hoạt hóa của phản ứng trên.
Cho hằng số tốc độ của một phản ứng là 11M-1.s-1 tại nhiệt độ 345 K và hằng số thực nghiệm Arrhenius là 20 M-1.s-1 . Tính năng lượng hoạt hóa của phản ứng trên.
Quảng cáo
Trả lời:
Áp dụng phương trình Arrhenius:
⇔ ⇒ Ea = 1715 kJ/mol
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Áp dụng phương trình Arrhenius viết lại cho hai nhiệt độ
T1 = 300K; T2 = 273K ứng với hai hằng số tốc độ k1 = 10-10s-1; k2 = ?
⇔
⇔ k2 = 1,23.10-12s-1
Vậy hằng số tốc độ phản ứng ở 273 K của phản ứng phân hủy là k2 = 1,23.10-12 s-1
Lời giải
a) Trong giản đồ (c) Ea’ là năng lượng hoạt hóa của phản ứng khi không có xúc tác.
Ea là năng lượng hoạt hóa của phản ứng khi có xúc tác.
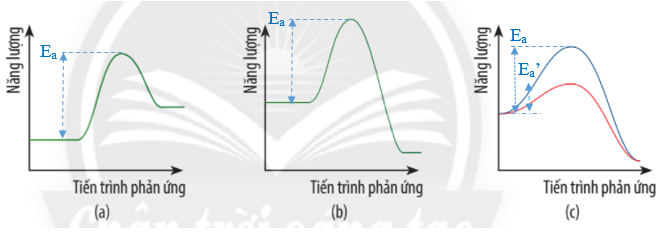
b) Giản đồ (c) biểu diễn ảnh hưởng của xúc tác đến năng lượng hoạt hóa của phản ứng.
Đường màu xanh là năng lượng hoạt hóa khi không có xúc tác.
Đường màu đỏ là năng lượng hoạt hóa khi có xúc tác.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.