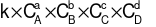Cho phản ứng:
2N2O5 (g) ⟶ O2 (g) + 4NO2 (g)
Sau thời gian từ giây 57 đến giây 116, nồng độ N2O5 giảm từ 0,4 M về 0,35 M. Tốc độ trung bình của phản ứng trong khoảng thời gian trên là
A. 8,48.10−4 M / giây;
B. 4,42.10−4 M / giây;
C. 8,84.10−4 M / giây;
D. 4,24.10−4 M / giây.
Quảng cáo
Trả lời:
Đáp án đúng là: D
Tốc độ trung bình của phản ứng trong khoảng thời gian từ giây 57 đến giây 116 là:
 =
= 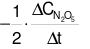 =
= 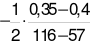 ≈ 4,24.10−4 (M / giây).
≈ 4,24.10−4 (M / giây).
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
A. bản chất của phản ứng;
B. nồng độ các chất;
C. nhiệt độ;
D. Cả A và C.
Lời giải
Đáp án đúng là: D
Hằng số tốc độ phản ứng k chỉ phụ thuộc vào bản chất của phản ứng và nhiệt độ.
Câu 2
A. đại lượng đặc trưng cho sự biến thiên nồng độ của chất phản ứng trong một đơn vị thời gian;
B. đại lượng đặc trưng cho sự biến thiên nồng độ của chất sản phẩm trong một đơn vị thời gian;
C. đại lượng đặc trưng cho sự biến thiên tốc độ chuyển động của chất phản ứng hoặc sản phẩm trong một đơn vị thời gian;
D. đại lượng đặc trưng cho sự biến thiên nồng độ của một trong các chất phản ứng hoặc sản phẩm trong một đơn vị thời gian,
Lời giải
Đáp án đúng là: D
Tốc độ phản ứng của một phản ứng hóa học là đại lượng đặc trưng cho sự biến thiên nồng độ của một trong các chất phản ứng hoặc sản phẩm trong một đơn vị thời gian.
Câu 3
A. tăng 3 lần;
B. tăng 6 lần;
C. tăng 9 lần;
D. tăng 81 lần.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
A. kí hiệu là 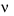 , đơn vị là (đơn vị nồng độ) / đơn vị thời gian;
, đơn vị là (đơn vị nồng độ) / đơn vị thời gian;
B. kí hiệu là  , đơn vị là (đơn vị khối lượng) / đơn vị thời gian;
, đơn vị là (đơn vị khối lượng) / đơn vị thời gian;
C. kí hiệu là 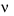 , đơn vị là (đơn vị nồng độ) / đơn vị thể tích;
, đơn vị là (đơn vị nồng độ) / đơn vị thể tích;
D. kí hiệu là  , đơn vị là (đơn vị khối lượng) / đơn vị thể tích.
, đơn vị là (đơn vị khối lượng) / đơn vị thể tích.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
A. 2,5.10−4 M/s;
B. 5.10−4 M/s;
C. 1,5.10−4 M/s;
D. 3.10−4 M/s.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
A. tăng gấp 4 lần
B. tăng gấp 8 lần
C. không thay đổi
D. giảm 2 lần
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.






















 O2 (s) +2H2O (l)
O2 (s) +2H2O (l)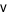 =
=