c) Kết quả thực nghiệm xác nhận giá trị enthalpy tạo thành chuẩn của khí ammonia là –45,9 kJ mol–1. Hãy cho biết vì sao có sự khác biệt về giá trị enthalpy tạo thành chuẩn của khí ammonia theo kết quả tính ở b) và kết quả thực nghiệm.
c) Kết quả thực nghiệm xác nhận giá trị enthalpy tạo thành chuẩn của khí ammonia là –45,9 kJ mol–1. Hãy cho biết vì sao có sự khác biệt về giá trị enthalpy tạo thành chuẩn của khí ammonia theo kết quả tính ở b) và kết quả thực nghiệm.
Câu hỏi trong đề: Giải SBT Hóa học 11 CD Bài 4: Đơn chất nitrogen có đáp án !!
Quảng cáo
Trả lời:
c) Giá trị enthalpy tạo thành chuẩn tính theo năng lượng liên kết thường khác biệt nhiều với giá trị thực nghiệm. Đó là do giá trị năng lượng của một liên kết cộng hoá trị giữa A và B thường chỉ là giá trị năng lượng liên kết trung bình của các liên kết giữa A và B trong nhiều hợp chất khác nhau. Trong bài tập này, giá trị 389 kJ mol–1 được hiểu là giá trị trung bình năng lượng liên kết N và H trong nhiều hợp chất khác nhau, như NH3, CH3–NH2,…
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án đúng là: A
Phân tử N2 hoạt động hoá học kém hơn Cl2 do năng lượng liên kết của N2 lớn hơn nhiều so với Cl2.
Lời giải
Đáp án đúng là: B
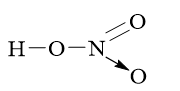
Công thức cấu tạo của HNO3 là:
Vậy N có cộng hóa trị là 4. Số oxi hóa của N là +5 (do trong HNO3 số oxi hóa của H là +1 và O là –2, áp dụng quy tắc xác định số oxi hoá xác định được số oxi hoá của N là +5).
Câu 3
Cho hai phương trình hoá học sau:
N2(g) + O2(g) ⟶ 2NO(g) = 180 kJ (1)
2NO(g) + O2(g) ⟶ 2NO2(g) = –114 kJ (2)
Những phát biểu nào sau đây về hai phương trình hoá học trên là đúng?
(a) Phản ứng (1) là phản ứng thu nhiệt, phản ứng (2) là phản ứng toả nhiệt.
(b) Phản ứng (2) tạo NO2 từ NO, là quá trình thuận lợi về mặt năng lượng. Điều này cũng phù hợp với thực tế là khí NO (không màu) nhanh chóng bị oxi hoá thành khí NO2 (màu nâu đỏ).
(c) Enthalpy tạo thành chuẩn của NO2 là 80 kJ mol–1.
(d) Từ giá trị biến thiên enthalpy chuẩn của phản ứng (1) và năng lượng liên kết trong phân tử O2, N2 lần lượt là 498 kJ mol–1 và 946 kJ mol–1, tính được năng lượng liên kết trong phân tử NO ở cùng điều kiện là 632 kJ mol–1.
Cho hai phương trình hoá học sau:
N2(g) + O2(g) ⟶ 2NO(g) = 180 kJ (1)
2NO(g) + O2(g) ⟶ 2NO2(g) = –114 kJ (2)
Những phát biểu nào sau đây về hai phương trình hoá học trên là đúng?
(a) Phản ứng (1) là phản ứng thu nhiệt, phản ứng (2) là phản ứng toả nhiệt.
(b) Phản ứng (2) tạo NO2 từ NO, là quá trình thuận lợi về mặt năng lượng. Điều này cũng phù hợp với thực tế là khí NO (không màu) nhanh chóng bị oxi hoá thành khí NO2 (màu nâu đỏ).
(c) Enthalpy tạo thành chuẩn của NO2 là 80 kJ mol–1.
(d) Từ giá trị biến thiên enthalpy chuẩn của phản ứng (1) và năng lượng liên kết trong phân tử O2, N2 lần lượt là 498 kJ mol–1 và 946 kJ mol–1, tính được năng lượng liên kết trong phân tử NO ở cùng điều kiện là 632 kJ mol–1.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















