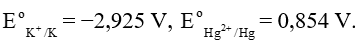Ở nhiệt độ thường, những kim loại nào có thể phản ứng được với dung dịch HCl 1 M, những kim loại nào có thể phản ứng được với H2O để tạo ra H2? Giải thích.
Ở nhiệt độ thường, những kim loại nào có thể phản ứng được với dung dịch HCl 1 M, những kim loại nào có thể phản ứng được với H2O để tạo ra H2? Giải thích.
Quảng cáo
Trả lời:
Ở nhiệt độ thường:
- Những kim loại có thể phản ứng được với dung dịch HCl 1 M là: Li, K, Ba, Ca, Na, Mg, Al, Zn, Cr, Fe, Ni, Sn, Pb…
- Những kim loại có thể phản ứng được với H2O để tạo ra H2 là: Li, K, Ba, Ca, Na…
Giải thích:
- Trong môi trường trung tính, có:
2H2O + 2e ⇌ H2 + 2OH- với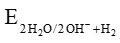 = – 0,413 V
= – 0,413 V
Cặp oxi hóa – khử Mn+/M của các kim loại Li, K, Ba, Ca, Na có giá trị thế điện cực chuẩn nhỏ hơn – 0,413 V nên các kim loại đó có thể tác dụng với nước ở nhiệt độ thường tạo thành hydroxide và khí hydrogen.
- Trong môi trường acid, có:
2H+ + 2e ⟶ H2 với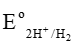 = 0 V
= 0 V
Cặp oxi hóa – khử Mn+/M của các kim loại Li, K, Ba, Ca, Na, Mg, Al, Zn, Cr, Fe, Ni, Sn, Pb có thế điện cực chuẩn nhỏ hơn 0 V có thể khử được ion H+ trong dung dịch acid tạo thành khí H2.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
a) Ta có:
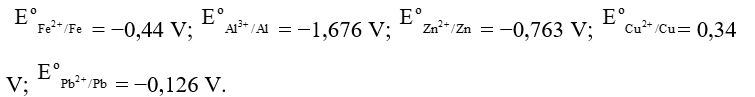
Như vậy sắt có thế điện cực chuẩn nhỏ hơn của đồng và chì.
Trường hợp có phản ứng tạo thành kim loại là:
+ Cho đinh sắt vào dung dịch copper(II) sulfate. Khi đó sắt (Fe) đóng vai trò là chất khử, copper(II) sulfate (CuSO4) đóng vai trò là chất oxi hóa.
+ Cho đinh sắt vào dung dịch lead(II) nitrate. Khi đó sắt (Fe) đóng vai trò là chất khử, lead(II) nitrate (Pb(NO3)2) đóng vai trò là chất oxi hóa.
b) Phương trình hoá học ở dạng ion thu gọn.
Fe(s) + Cu2+(aq) ⟶ Fe2+(aq) + Cu(s)
Fe(s) + Pb2+(aq) ⟶ Fe2+(aq) + Pb(s)
Lời giải
- Hiện tượng: Xuất hiện lớp chất rắn màu đỏ bám trên đinh sắt, màu xanh của dung dịch nhạt dần.
- Giải thích: Sản phẩm thu được là Cu ở thể rắn và có màu đỏ. CuSO4 đã tham gia phản ứng nên nồng độ giảm dần làm cho màu dung dịch nhạt dần đi.
+ Phương trình hóa học:
Fe(s) + CuSO4 (aq) ⟶ FeSO4 (aq) + Cu(s)
+ Do = −0,44 V < = 0,34 V nên sắt dễ dàng đẩy đồng ra khỏi dung dịch copper(II) sulfate.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.