Hòa tan 2,80 gam một loại quặng sắt (E) trong dung dịch H2SO4 loãng, thu được dung dịch X (gồm các hợp chất của sắt) và chất rắn Y (không chứa nguyên tố sắt). Cho kim loại Cu tan vào X, thu được dung dịch Z chứa hai muối rồi pha loãng Z thu được dung dịch T. Cho T phản ứng vừa đủ với 20,00 ml dung dịch KMnO4 0,05M trong dung dịch H2SO4. Phần trăm khối lượng nguyên tố sắt có trong quặng sắt (E) là
Câu hỏi trong đề: (2024) Đề minh họa tham khảo BGD môn Hóa có đáp án (Đề 16) !!
Quảng cáo
Trả lời:
Cho Cu vào X thu được Z chứa 2 muối là CuSO4 và FeSO4 nên X gồm Fe2(SO4)3, FeSO4
Bảo toàn e: \[{n_{FeS{O_4}}} = {\rm{ }}5{n_{KMn{O_4}}}\] = 5.10-3 mol
Bảo toàn Fe: nFe (E) = \[{n_{FeS{O_4}}}\] = 5.10-3 mol Þ \[\% {m_{Fe}} = \frac{{{{5.10}^{ - 3}}.56}}{{2,80}}.100 = 10\% \]
Hot: 1000+ Đề thi giữa kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
- 500 Bài tập tổng ôn Hóa học (Form 2025) ( 38.000₫ )
- 1200 câu hỏi lí thuyết Hóa học (Form 2025) ( 38.000₫ )
- Bộ đề thi tốt nghiệp 2025 các môn Toán, Lí, Hóa, Văn, Anh, Sinh, Sử, Địa, KTPL (có đáp án chi tiết) ( 36.000₫ )
- Tổng ôn lớp 12 môn Toán, Lí, Hóa, Văn, Anh, Sinh Sử, Địa, KTPL (Form 2025) ( 36.000₫ )
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
Lời giải
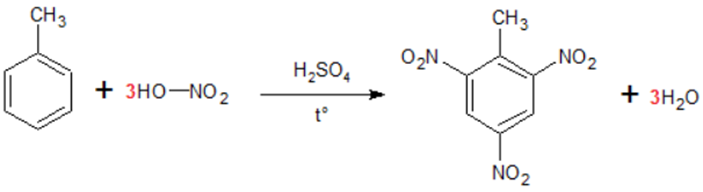
Số mol C6H2(NO2)3CH3 = \(\frac{{40}}{{227}}\;kmol \Rightarrow {m_{{C_7}{H_8}}} = \frac{{40}}{{227}}.\frac{{100}}{{70\% }}.92 = 23,16\;kg\)
Để có được 2500 bao thuốc nổ TNT thì cần 23,16.2500 = 57898 kg = 57,898 tấn toluen
Lời giải
AlCl3 + 3NH3 + 3H2O ® Al(OH)3 + 3NH4Cl
(1): Al(OH)3 + 3HCl ® AlCl3 + 3H2O
(2): Al(OH)3 + NaOH ® NaAlO2 + 2H2O
(a) Đúng.
(b) Đúng, kết tủa tan tạo dung dịch trong suốt.
(c) Sai, kết tủa tan tạo dung dịch trong suốt.
(d) Sai, AlCl3 không có tính chất lưỡng tính..
(e) Sai, nếu thay NaOH thì ở bước 2 không thu được kết tủa.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.