Công thức tính biến thiên enthalpy của phản ứng theo năng lượng liên kết (trong đó, kí hiệu 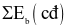 là tổng năng lượng liên kết của các chất tham gia phản ứng; kí hiệu
là tổng năng lượng liên kết của các chất tham gia phản ứng; kí hiệu 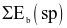 là tổng năng lượng liên kết của các chất sản phẩm phản ứng) là
là tổng năng lượng liên kết của các chất sản phẩm phản ứng) là
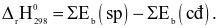
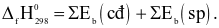
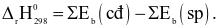
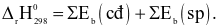
Câu hỏi trong đề: Đề kiểm tra Hóa 10 Kết nối tri thức Chương 5 có đáp án !!
Quảng cáo
Trả lời:
Đáp án đúng là: C
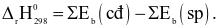
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
không có sự thay đổi năng lượng.
có sự hấp thụ nhiệt lượng từ môi trường xung quanh.
thu nhiệt.
tỏa nhiệt.
Lời giải
Đáp án đúng là: D
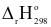 = -571,68kJ > 0 ⇒ phản ứng tỏa nhiệt.
= -571,68kJ > 0 ⇒ phản ứng tỏa nhiệt.
Câu 2
Cho giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn:
| Liên kết | C – H | C – C | C = C |
| E b (kJ/mol) | 418 | 346 | 612 |
Lời giải
Đáp án đúng là: +80.
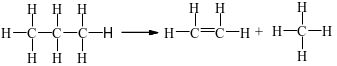
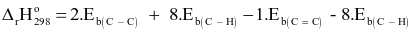
= 2.346 + 8.418 - 1.612 - 8.418 = +80 kJ.
Câu 3
Cho phản ứng đốt cháy octane như sau:
C8H18 (g) + 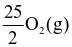 → 8CO2 (g) + 9H2O (l)
→ 8CO2 (g) + 9H2O (l) 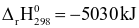
Cho giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn:
| Liên kết | C – H | C – C | O = O | C = O | H - O |
| E b (kJ/mol) | 414 | 347 | 498 | 799 | x |
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
NaCl(s).
CO2(g).
H2O(l).
H2(g).
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
46 kJ.
92 kJ.
-46 kJ.
- 92 kJ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.






















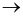 2H2O(l)
2H2O(l)  Fe3O4(s) + 4H2(g)
Fe3O4(s) + 4H2(g) 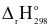 = +26,32 kJ
= +26,32 kJ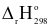 = +179,20 kJ
= +179,20 kJ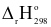 = ‒285,66 kJ
= ‒285,66 kJ ZnO(s) + SO3(g) ;
ZnO(s) + SO3(g) ; 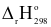 = + 235,21 kJ
= + 235,21 kJ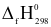 ) bằng 0 (kJ/mol)?
) bằng 0 (kJ/mol)? ZnSO4(s)
ZnSO4(s) 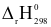 =
= 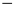 235,21 kJ
235,21 kJ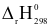 =
= 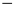 367,50 kJ
367,50 kJ CO(g) +
CO(g) + 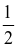 O2(g)
O2(g) 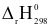 = +280,00 kJ
= +280,00 kJ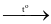 3CO2(g) + 4H2O (l)
3CO2(g) + 4H2O (l) 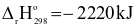
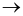 2NH3(g)
2NH3(g)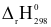 = -92 kJ
= -92 kJ