Nhiệt độ sôi của các hydrogen halide được biểu diễn qua đồ thị sau:
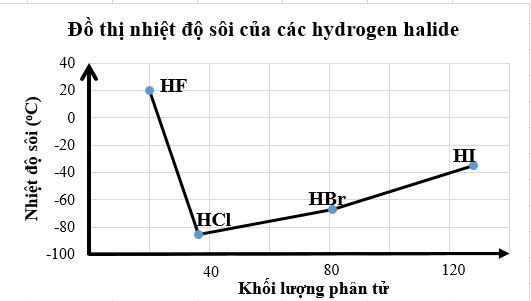
(a) Các phân tử hydrogen fluoride hình thành liên kết hydrogen liên phân tử nên nhiệt độ sôi của hydrogen fluoride cao bất thường so với các hydrogen halide còn lại.
(b) Nhiệt độ sôi của hydrogen fluoride cao bất thường so với các hydrogen halide còn lại là do lực tương tác van der Waals của HF lớn hơn.
(c) Nhiệt độ sôi tăng dần từ HF đến HI do khối lượng phân tử tăng dẫn đến tương tác van der Waals tăng.
(d) Nhiệt độ sôi của các hydrogen halide tăng dần từ HCl đến HI là do khối lượng phân tử tăng dẫn đến liên kết hydrogen liên phân tử tăng dần.
Câu hỏi trong đề: Đề kiểm tra Hóa 10 Kết nối tri thức Chương 7 có đáp án !!
Quảng cáo
Trả lời:
(a) Đúng.
(b) Sai. Nhiệt độ sôi của hydrogen fluoride cao bất thường so với các hydrogen halide còn lại là do các phân tử hydrogen fluoride hình thành liên kết hydrogen liên phân tử.
(c) Sai. HF có nhiệt độ sôi cao nhất trong dãy.
(d) Sai. Nhiệt độ sôi của các hydrogen halide tăng dần từ HCl đến HI là do khối lượng phân tử tăng dẫn đến tương tác van der Walls giữa các phân tử tăng dần.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
(a) Đúng.
(b) Đúng.
(c) Đúng.
(d) Sai. X là hydrochloric acid và là một acid mạnh.
Lời giải
Đáp án đúng là: 4.
Lượng muối I - ốt một người trưởng thành cần trong một ngày là: 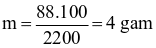
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
Các nguyên tố phổ biến thuộc nhóm halogen (VIIA) trong bảng tuần hoàn các nguyên tố hóa học gồm: F (Z = 9), Cl (Z = 17), Br (Z = 35) và I (Z = 53). Đơn chất halogen tồn tạo dạng phân tử  giữa các phân tử
giữa các phân tử  thường có tương tác với nhau. Cho giá trị năng lượng liên kết
thường có tương tác với nhau. Cho giá trị năng lượng liên kết 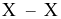 ở bảng sau:
ở bảng sau:
| Liên kết | F - F | Cl - Cl | Br - Br | I - I |
Năng lượng liên kết (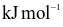 ) )
ở | 159 | 243 | 193 | 151 |
(a) Cấu hình electron lớp ngoài cùng của nguyên tử X có dạng 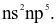
(b) Liên kết giữa các nguyên tử trong 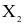 là liên kết cộng hóa trị không phân cực.
là liên kết cộng hóa trị không phân cực.
(c) Tương tác giữa các phân tử 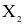 là tương tác van der Waals.
là tương tác van der Waals.
(d) Năng lượng liên kết Cl – Cl lớn nhất trong dãy trên vì Cl có bán kính nguyên tử nhỏ nhất.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
F2.
Cl2.
Br2.
I2.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.






















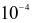 đến
đến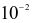 mol/L, đóng vai trò quan trọng trong quá trình tiêu hoá, cùng với enzyme và sự co bóp của cơ dạ dày nhằm chuyển hoá thức ăn thành chất dinh dưỡng cho cơ thể dễ hấp thụ.
mol/L, đóng vai trò quan trọng trong quá trình tiêu hoá, cùng với enzyme và sự co bóp của cơ dạ dày nhằm chuyển hoá thức ăn thành chất dinh dưỡng cho cơ thể dễ hấp thụ.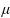 g; lượng iodide cần thiết cho một người trưởng thành khoảng 88
g; lượng iodide cần thiết cho một người trưởng thành khoảng 88 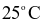 và 1 bar
và 1 bar