Hợp chất KMnO4 có thể được điều chế từ MnO2 theo các bước sau :
• Bước 1: Đun nóng hỗn hợp gồm KClO3, KOH và 30,20 gam MnO2 trong chén nickel để thực hiện phản ứng: 3MnO2 + KClO3 + 6KOH → 3K2MnO4 + KCl + 3H2O (1)
• Bước 2: Để nguội hỗn hợp, cho nước vào chén nickel, khuấy đều, lọc lấy phần dung dịch. Tiếp đó, sục khí Cl2 dư vào dung dịch nước lọc: 2K2MnO4 + Cl2 → 2KMnO4 + 2KCl (2)
• Bước 3: Làm lạnh để sản phẩm kết tinh, lọc thu lấy tinh thể, sấy khô, thu được 49,95 gam sản phẩm X gồm KMnO4 có lẫn một lượng nhỏ KCl.
Để xác định hiệu suất tổng hợp và độ tinh khiết của sản phẩm KMnO4 thu được ở trên, người ta hòa tan 1,6 gam X vào nước và định mức thành 50 mL dung dịch Y. Chuyển Y lên burette để thực hiện quá trình chuẩn độ 10,0 mL dung dịch H2C2O4 0,5M thì cần vừa đủ 10,0 mL dung dịch Y theo phản ứng :
5H2C2O4 + 2KMnO4 + 3H2SO4 → 10CO2 + K2SO4 + 2MnSO4 + 8H2O (3)
Hiệu suất quá trình tổng hợp KMnO4 và độ tinh khiết của KMnO4 trong X lần lượt là x và y (x, y được làm tròn đến hàng đơn vị). Hãy tính tổng (x + y). (KCl nồng độ nhỏ coi như không có phản ứng với dung dịch KMnO4/H2SO4).
Quảng cáo
Trả lời:
Đáp án:
Đáp án: 189
nH2C2O4 = 5 mmol → nKMnO4 (10 mL Y) = 2 mmol
→ nKMnO4 (1,6 gam X) = nKMnO4 (50 mL Y) = 10 mmol
→ y = 10.158/(1,6.1000) = 98,75%
nMnO2 phản ứng = nKMnO4 (49,95 gam X) = 49,95.10/1,6 = 312,1875 mmol
→ x = 312,1875.87/(30,20.1000) = 89,93%
→ x + y = 188,68% ≈ 189%
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
a. Công thức của muối chloride ngậm nước (X) là FeCl2.6H2O.
b. Trong các phức chất [M(H2O)6]2+, [MCl4]2- các phối tử đều có dung lượng phối trí là 1.
c. Ngâm ống thứ nhất vào nước lạnh, dung dịch trong đó sẽ chuyển sang màu hồng.
d. Cho vài giọt dung dịch AgNO3 0,1M vào ống thứ hai, kết tủa thu được là hỗn hợp gồm Ag và AgCl.
Lời giải
a) Sai, X dạng MClx.kH2O
mM/mCl = M/(35,5x) = 24,79/29,83
→ M = 29,5x
Chọn x = 2, M = 59: M là Ni
nNi : nO = 1 : k = 24,79/59 : 40,35/16 → k = 6
X là NiCl2.6H2O
b) Đúng, các phối tử H2O hoặc Cl- trong phức chất [Ni(H2O)6]2+, [NiCl4]2- đều có dung lượng phối trí là 1.
c) Đúng, cân bằng trên có chiều thuận thu nhiệt nên khi ngâm vào nước lạnh (giảm nhiệt độ) cân bằng sẽ chuyển dịch theo chiều nghịch. Do đó dung dịch sẽ chuyển từ màu xanh (xuất hiện từ lúc thêm HCl đặc trước đó) sang màu hồng.
d) Sai, kết tủa chỉ có AgCl do:
NiCl2 + 2AgNO3 → 2AgCl + Ni(NO3)2
Lời giải
Đáp án:
Đáp án: 3,2
4 tấn gang (3,8 tấn Fe + 0,2 tấn C) + m tấn phế liệu (0,5m tấn Fe3O4 + 0,49m tấn Fe + 0,01m tấn C) → a tấn thép (0,99a tấn Fe + 0,01a tấn C)
Bảo toàn Fe:
3,8 + 56.3.0,5m/232 + 0,49m = 0,99a (1)
Fe3O4 + 2C → 3Fe + 2CO2
mC phản ứng = 0,5m.12.2/232 = 3m/58
Bảo toàn C:
0,2 + 0,01m = 3m/58 + 0,01a (2)
(1)(2) → m = 3,2; a = 6,6
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
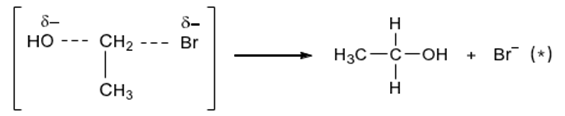
Trong phân tử ethyl bromide, liên kết C−Br phân cực nên dễ bị phân cắt.
Trong giai đoạn (∗), có sự phá vỡ một liên kết σ và hình thành một liên kết π mới.
Giai đoạn (∗) biểu diễn sự chuyển hóa chất tham gia phản ứng thành trạng thái chuyển tiếp.
Phản ứng (1) thuộc loại phản ứng trao đổi.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
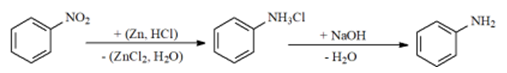
Trong phản ứng khử nitrobenzene bằng (Zn + HCl), tác nhân khử là hydrogen mới sinh [H].
Trong phản ứng ở giai đoạn (2), cation C6H5NH3+ là một base theo thuyết Brønsted – Lowry.
Theo sơ đồ tổng hợp aniline ở trên, từ 61,5 gam nitrobenzene có thể thu được 37,2 gam aniline, với hiệu suất của quá trình tổng hợp aniline từ nitrobenzene là 80%.
Phương pháp có thể sử dụng để tách aniline ra khỏi hỗn hợp sau kiềm hóa là phương pháp chiết lỏng – lỏng. Aniline dễ dàng được chiết tách ra khỏi pha nước bằng các dung môi hữu cơ như ether, benzene hoặc dichloromethane.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.