Ester no, đơn chức, mạch hở (X) là dung môi hữu cơ được sử dụng nhiều trong công nghiệp hoá chất. Phổ MS của X cho biết khối lượng phân tử là 88. Trong đời sống, hợp chất X2 được điều chế từ quá trình lên men tinh bột và là một thành phần của xăng E5. Cho các phương trình hoá học sau:
(1) X + NaOH → X1 + X2.
(2) X2 + CuO → X3 + Cu + H2O.
(3) X3 + Br2 + H2O → X4 + HBr
Phát biểu nào sau đây là đúng?
X và X4 là hai chất đồng phân.
X tan tốt trong nước hơn X1 và X2.
Thứ tự nhiệt độ sôi được sắp xếp theo chiều X2 < X3 < X4.
Có thể thực hiện phản ứng theo sơ đồ chuyển hoá X2 → X4 → X.
Quảng cáo
Trả lời:
Đáp án đúng là: D
MX = 88 → X là C4H8O2.
X2 được điều chế từ quá trình lên men tinh bột và là một thành phần của xăng E5 → X2 là C2H5OH
→ X là CH3COOC2H5; X1 là CH3COONa; X3 là CH3CHO; X4 là CH3COOH.
- Phát biểu A sai, X và X4 có công thức phân tử khác nhau nên không phải đồng phân.
- Phát biểu B sai, X là ester nhỏ nên có độ tan trung bình (nồng độ bão hòa khoảng 8%), X1 và X2 tan rất tốt.
- Phát biểu C sai, acid có liên kết H liên phân tử bền hơn alcohol; trong khi aldehyde không có liên kết hydrogen liên phân tử nên nhiệt độ sôi CH3CHO < C2H5OH < CH3COOH.
- Phát biểu D đúng:
C2H5OH + O2 → CH3COOH + H2O (đk: lên men giấm)
CH3COOH + C2H5OH ⇌ CH3COOC2H5 + H2O (đk: H2SO4 đặc, t°)
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án:
Đáp án: 6,77
(1) MnO4-(aq) + 4H+(aq) + 3Fe2+(aq) → MnO2(s) + 3Fe3+(aq) + 2H2O(l)
(2) MnO4-(aq) + 8H+(aq) + 5Fe2+(aq) → Mn2+(aq) + 5Fe3+(aq) + 4H2O(l)
Thao tác đúng (chỉ có phản ứng (2)):
.
Thao tác sai (có cả phản ứng (1) và (2)):
Đặt, gồm 0,55x mol tham gia (1) và 0,45x mol tham gia (2):
→ Thể tích KMnO4 0,02M đã tăng =
Lời giải
Đáp án:
Đáp án: 3
α-amino acid là chất có nhóm -NH2 gắn vào carbon số 2. Các chất là α-amino acid gồm:
(Aspartic acid).
(Alanine).
(Glycine).
Câu 3
Công thức phân tử của acetic acid là C2H6O2.
Giấm ăn có pH < 7.
Có thể dùng giấm ăn để làm mất mùi tanh của cá khi ta chế biến các món ăn.
Nồng độ phần trăm acetic acid trong dung dịch thu được sau phản ứng lên men là 4,03%.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
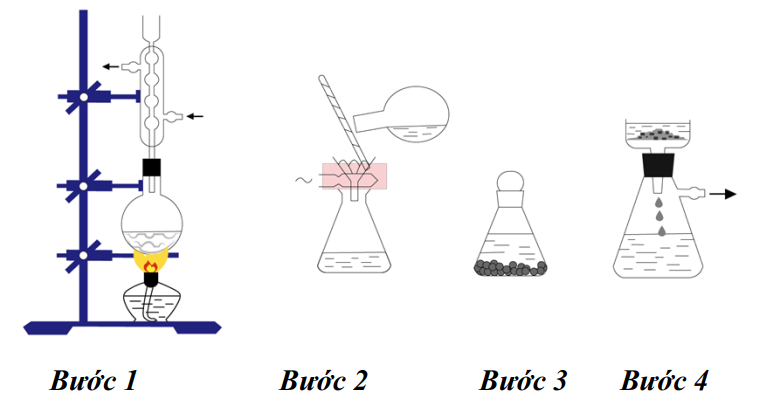
Sắc kí cột.
Chiết.
Kết tinh.
Chưng cất.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
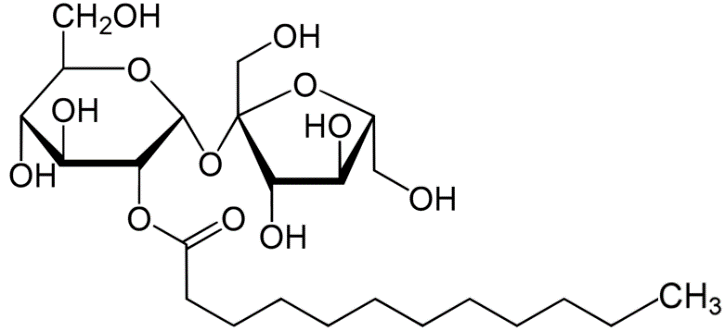
a. Lauric acid có chứa 12 nguyên tử carbon trong phân tử.
b. Saccharose monolaurate có đầu ưa nước là gốc saccharose và đuôi kị nước là gốc hydrocarbon.
c. Thuỷ phân hoàn toàn saccharose monolaurate trong môi trường acid thu được hai sản phẩm hữu cơ.
d. Trong saccharose monolaurate, gốc laurate gắn với nguyên tử C số 2 ở gốc glucose.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
X2 có trong thành phần của xăng E5.
Các dung dịch X1 và X2 đều hoà tan được Cu(OH)2 trong môi trường kiềm ở điều kiện thường tạo thành dung dịch màu xanh lam.
Phản ứng (1) và (2) đều là phản ứng thuỷ phân trong môi trường acid.
X3 được sử dụng trong việc bảo quản hoa quả tươi.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.