Nguyên tố Mg có 3 loại đồng vị có số khối lần lượt là: 24, 25 và 26. Trong 5000 nguyên tử Mg thì có 3930 đồng vị 24, 505 đồng vị 25, còn lại là đồng vị 26. Hãy tính khối lượng nguyên tử trung bình của Mg.
A. 24,998
B. 25,527
C.25,103
D. 24,327
Câu hỏi trong đề: ĐGNL ĐHQG TP.HCM - Vấn đề thuộc lĩnh vực hóa học - Đồng vị !!
Quảng cáo
Trả lời:
Trả lời:
% Mg ( 24 ) = 3930 : 5000 . 100% = 78,6 %
% Mg ( 25 ) = 505 : 5000 . 100% = 10,1 %
% Mg ( 26 ) = 100 – 78,6 – 10,1 = 11,3 %
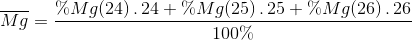
= 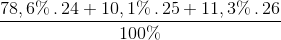
= 24,327
Đáp án cần chọn là: D
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Trả lời:
Gọi A2 là số khối của nguyên tử dồng vị thứ 2.
Ta có:
\[\frac{{79.54,5 + {A_2}\left( {100 - 54,5} \right)}}{{100}} = 79,91\]
=>4305,5 + 45,5A2 = 7991
=>45,5A2 = 7991 − 4305,5
=>45,5A2 = 3685,5
=>A2 = 81
Đáp án cần chọn là: D
Câu 2
A. 3,07%.
B. 14,42%.
C. 8,91%.
D. 12,22%
Lời giải
Trả lời:
\[{\overline A _B} = \frac{{{x_1}.{A_1} + {x_2}.{A_2}}}{{100}}\]
\[ \to {\overline A _B} = \frac{{{x_1}.10 + \left( {100 - {x_1}} \right).11}}{{100}} = 10,81\]
\[ \to {x_1} = 19\% \]
+) Lấy 1 mol H3BO3 (61,81 gam) trong đó có chứa 1 mol B
=>có 0,19 mol 10B và 0,81 mol 11B
=>khối lượng 11B = 0,81.11 = 8,91
\[ \Rightarrow \% {m_{{{11}_B}}} = \frac{{{m_{{{11}_B}}}}}{{{m_{{H_3}P{O_3}}}}}.100\% \]
\[ \Rightarrow \% {m_{{{11}_B}}} = \frac{{8,91}}{{61,81}}.100\% \]
\[ \Rightarrow \% {m_{{{11}_B}}} = 14,42\% \]
Đáp án cần chọn là: B
Câu 3
A. 35,48
B. 35,05
C. 36,00
D. 36,52
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
A. 98,9% và 1,1%
B. 49,5% và 51,5%
C. 99,8% và 0,2%
D. 75% và 25%
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















