Cho m gam hỗn hợp G gồm Mg và Al có tỉ lệ mol 4 : 5 vào dung dịch HNO3 20%. Sau khi các kim loại tan hết có 6,72 lít hỗn hợp X gồm NO, N2O, N2 bay ra (đktc) và được dung dịch T. Thêm một lượng O2 vừa đủ vào X, sau phản ứng được hỗn hợp khí Y. Dẫn Y từ từ qua dung dịch KOH dư, có 4,48 lít hỗn hợp khí Z đi ra (đktc). Tỉ khối của Z đối với H2 bằng 20. Nếu cho dung dịch NaOH vào dung dịch T thì lượng kết tủa lớn nhất thu được là (m + 39,1) gam. Biết HNO3 dùng dư 20% so với lượng cần thiết. Nồng độ phần trăm của Al(NO3)3 trong T gần nhất với
A. 9,5%
B. 9,6%
C. 9,4%
D. 9,7%
Quảng cáo
Trả lời:
Trả lời:
Khi thêm O2 vừa đủ vào Y thu được các khí NO2, N2O, N2. Dẫn qua dung dịch KOH dư thì NO2 bị hấp thụ khí còn lại là N2O và N2.
=>nNO = nNO2 = 0,3 – 0,2 = 0,1 mol
Áp dụng đường chéo cho hỗn hợp Z:
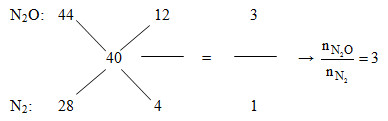
Mà nN2O + nN2 = nZ = 0,2 mol
=>nN2O = 0,15 và nN2 = 0,05
Đặt: nMg = 4x và nAl = 5x (mol)
=>nMg(OH)2 = 4x và mAl(OH)3 = 5x
m kết tủa max = mKL + mOH-
=>m + 39,1 = m + 17(4x.2 + 5x.3)
=>x = 0,1
=>nMg = 0,4 mol và nAl = 0,5 mol
Ta thấy:
2nMg + 3nAl >3nNO + 8nN2O + 10nN2
=>Có tạo muối NH4NO3
Bảo toàn e:
2nMg + 3nAl = 3nNO + 8nN2O + 10nN2 + 8nNH4NO3
=>2.0,4 + 3.0,5 = 3.0,1 + 8.0,15 + 10.0,05 + 8nNH4NO3
=>nNH4NO3 = 0,0375 mol
Công thức tính nhanh:
nHNO3pư = 4nNO + 10nN2O + 12nN2 + 10nNH4NO3 = 2,875 mol
=>nHNO3bđ = 2,875 + 2,875.(20/100) = 3,45 mol
=>m dd HNO3 = 3,45.63.(100/20) = 1086,75 gam
m dd sau pư = mMg + mAl + m dd HNO3 – mNO – mN2O – mN2
= 0,4.24 + 0,5.27 + 1086,75 – 0,1.30 – 0,15.44 – 0,05.28
= 1098,85 gam
Ta có: nAl(NO3)3 = nAl = 0,5 mol
→ %mAl = (0,5.213/1098,85).100% = 9,69% gần nhất với 9,7%
Đáp án cần chọn là: D
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
A. 1 : 2.
B. 1 : 10.
C. 1 : 9.
D. 1 : 3.
Lời giải
Trả lời:
\[\mathop {Fe}\limits^{ + 2} O + H\mathop N\limits^{ + 5} {O_3} \to \mathop {Fe}\limits^{ + 3} {\left( {N{O_3}} \right)_3} + \mathop N\limits^{ + 2} O + {H_2}O\]
\[3.\left| {\mathop {Fe}\limits^{ + 2} } \right. \to \mathop {Fe}\limits^{ + 3} + 1e\]
\[1.\left| {\mathop N\limits^{ + 5} } \right. + 3e \to \mathop N\limits^{ + 2} \]
=>PTHH: 3FeO + 10HNO3 → 3Fe(NO3)3 + NO + 5H2O
=>trong 10 phân tử HNO3 phản ứng, có 1 phân tử là chất oxi hóa tạo NO, 9 phân tử làm môi trường tạo muối Fe(NO3)3
Đáp án cần chọn là: C
Câu 2
A. Axit H2SO4 có tính axit mạnh hơn HNO3.
B. HNO3 dễ bay hơi hơn.
C.H2SO4 có tính oxi hoá mạnh hơn HNO3.
D. Một nguyên nhân khác.
Lời giải
Trả lời:
Vì HNO3 dễ bay hơi =>làm giảm lượng HNO3 trong bình =>phản ứng làm tăng lượng HNO3 (chiều thuận)
Đáp án cần chọn là: B
Câu 3
A. CaCO3, Cu(OH)2, Fe(OH)2, FeO.
B. CuO, NaOH, FeCO3, Fe2O3.
C. Fe(OH)3, Na2CO3, Fe2O3, Cu(OH)2.
D. KOH, FeS, K2CO3, Cu(OH)2
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
A. 44 : 6 : 9.
B. 46 : 9 : 6.
C.46 : 6 : 9.
D. 44 : 9 : 6.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
A. Tạo ra khí có màu nâu.
B. Tạo ra dung dịch có màu vàng.
C. Tạo ra kết tủa có màu vàng.
D. Tạo ra khí không màu, hoá nâu trong không khí.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
A. Nút ống nghiệm bằng bông tẩm nước.
B. Nút ống nghiệm bằng bông tẩm cồn
C. Nút ống nghiệm bằng bông tẩm giấm.
D. Nút ống nghiệm bằng bông tẩm xút.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















