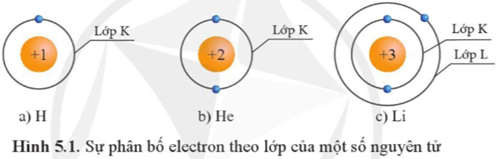
Dự đoán tính chất hóa học cơ bản (tính kim loại, tính phi kim, tính trơ) của các nguyên tố có Z từ 1 đến 20.
Câu hỏi trong đề: Bài tập Lớp, phân lớp và cấu hình electron có đáp án !!
Quảng cáo
Trả lời:
|
Số hiệu nguyên tử (Z) |
Cấu hình electron |
Tính chất hóa học cơ bản |
|
1 |
1s1 |
Tính kim loại |
|
2 |
1s2 |
Tính kim loại |
|
3 |
1s22s1 |
Tính kim loại |
|
4 |
1s22s2 |
Tính kim loại |
|
5 |
1s22s22p1 |
Tính phi kim |
|
6 |
1s22s22p2 |
Tính phi kim |
|
7 |
1s22s22p3 |
Tính phi kim |
|
8 |
1s22s22p4 |
Tính phi kim |
|
9 |
1s22s22p5 |
Tính phi kim |
|
10 |
1s22s22p6 |
Khí hiếm (tính trơ) |
|
11 |
1s22s22p63s1 |
Tính kim loại |
|
12 |
1s22s22p63s2 |
Tính kim loại |
|
13 |
1s22s22p63s23p1 |
Tính kim loại |
|
14 |
1s22s22p63s23p2 |
Tính phi kim |
|
15 |
1s22s22p63s23p3 |
Tính phi kim |
|
16 |
1s22s22p63s23p4 |
Tính phi kim |
|
17 |
1s22s22p63s23p5 |
Tính phi kim |
|
18 |
1s22s22p63s23p6 |
Khí hiếm (Tính trơ) |
|
19 |
1s22s22p63s23p64s1 |
Tính kim loại |
|
20 |
1s22s22p63s23p64s2 |
Tính kim loại |
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Nitrogen có Z = 7 = số electron
7 electron được phân bố vào 2 lớp:
+ Lớp thứ nhất chứa 2 electron, phân bố vào 1 AO.
+ Lớp thứ hai chứa 5 electron, phân bố vào 4 AO.
Như vậy lớp ngoài cùng của nitrogen chứa 5 electron, phân bố vào 4 AO.
Lời giải
Cấu hình electron theo orbital của nguyên tố X có thể là
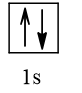
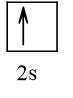
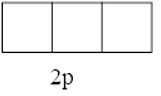
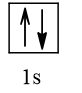
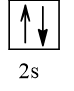
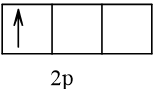
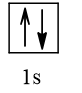
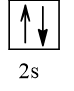
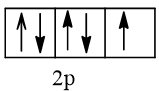
Vậy X có thể là Z = 3 (Li) hoặc Z = 5 (Bo) hoặc Z = 9 (F).
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.