Làm thế nào có thể so sánh sự nhanh, chậm của các phản ứng hoá học để thúc đẩy hoặc kìm hãm nó theo mong muốn?
Làm thế nào có thể so sánh sự nhanh, chậm của các phản ứng hoá học để thúc đẩy hoặc kìm hãm nó theo mong muốn?
Câu hỏi trong đề: Bài tập Tốc độ phản ứng có đáp án !!
Quảng cáo
Trả lời:
Để so sánh sự nhanh, chậm của các phản ứng hóa học, chúng ta có thể dựa vào tốc độ phản ứng hóa học.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
a) Phương trình tốc độ của phản ứng: v = k.CX.CY
b) Tốc độ phản ứng tại thời điểm đầu là:
v = 2,5.10-4.0,02.0,03 = 1,5.10-7 (mol/(L.s))
- Tại thời điểm đã hết một nửa lượng X
⇒ Nồng độ X còn 0,01M và đã phản ứng 0,01M
⇒ Theo phương trình, nồng độ Y phản ứng là 0,01M
⇒ Tại thời điểm xét, nồng độ Y còn 0,03M – 0,01M = 0,02M
⇒ v = 2,5.10-4.0,01.0,02 = 5.10-8 (mol/(L.s))
Lời giải
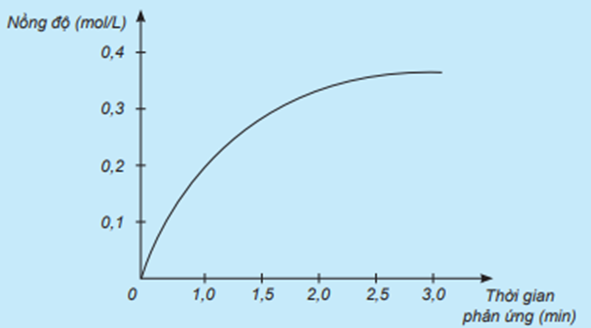
a) Đồ thị trên mô tả sự thay đổi nồng độ theo thời gian của HCl vì nồng độ của HCl tăng dần từ 0 mol/L theo thời gian.
b) Đơn vị của tốc độ phản ứng trong trường hợp này là mol/(L.min).
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.