Đồ thị nào sau đây thể hiện đúng sự thay đổi nhiệt độ khi dung dịch hydrochloric acid được cho vào dung dịch sodium hydroxide tới dư?
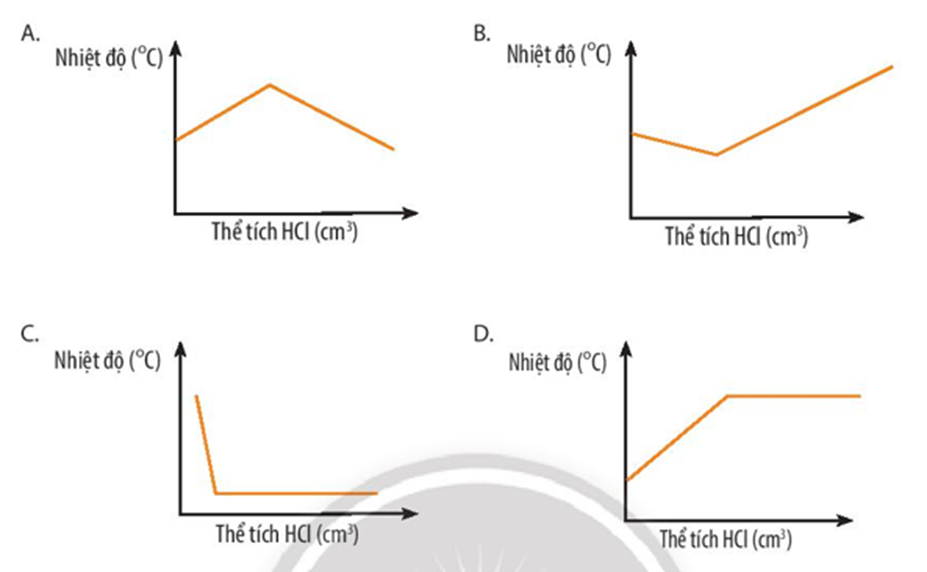
Đồ thị nào sau đây thể hiện đúng sự thay đổi nhiệt độ khi dung dịch hydrochloric acid được cho vào dung dịch sodium hydroxide tới dư?

Quảng cáo
Trả lời:
Đáp án đúng là: A
Phản ứng giữa hydrochloric acid (HCl) và sodium hydroxide (NaOH) là phản ứng tỏa nhiệt (∆ r= -57,3 kJ).
Khi hydrochloric acid (HCl) phản ứng với sodium hydroxide (NaOH) nhiệt độ tăng dần. Đến khi phản ứng kết thúc, nhiệt độ sẽ giảm dần để cân bằng với nhiệt độ môi trường.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án đúng là: D
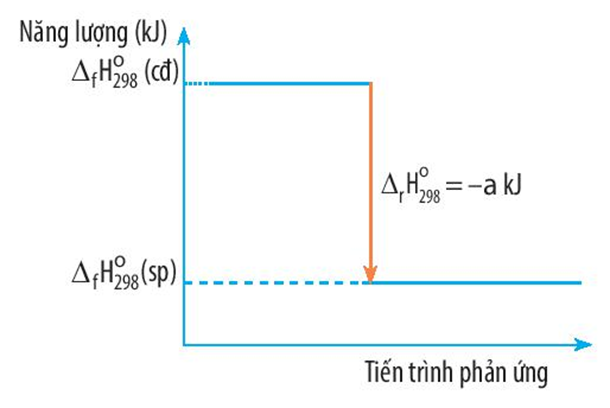
∆ r= +180 kJ > 0
⇒ Phản ứng hóa học xảy ra có sự hấp thụ nhiệt năng từ môi trường
Lời giải
Đáp án đúng là: A
Phản ứng có biến thiên enthalpy là ∆ r = -a kJ < 0 ⇒ Phản ứng tỏa nhiệt
Năng lượng chất tham gia phản ứng lớn hơn năng lượng chất sản phẩm.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.