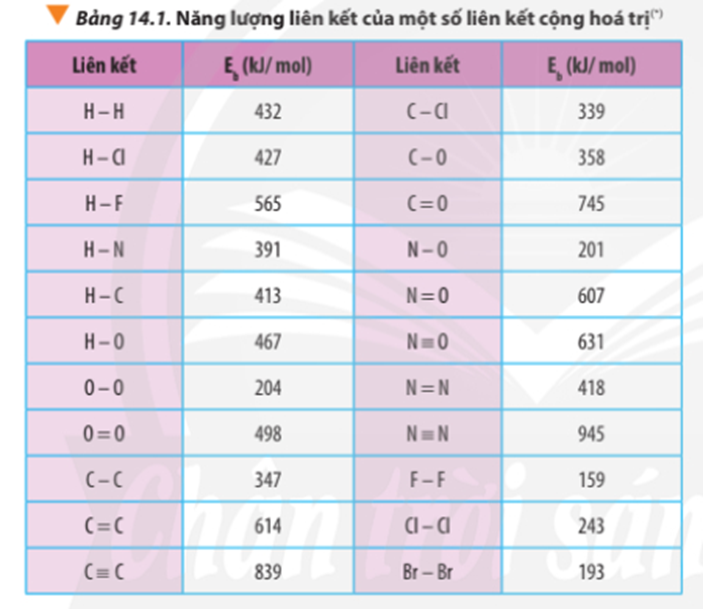
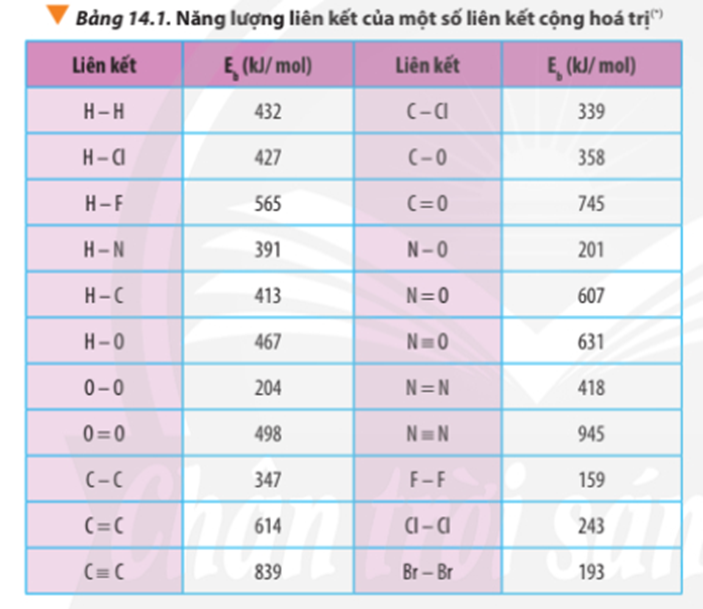
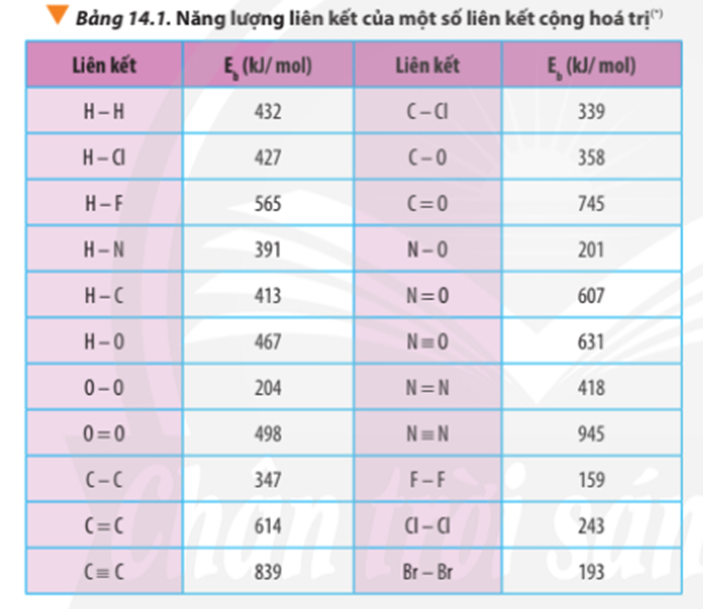
Dựa vào số liệu về năng lượng liên kết ở Bảng 14.1, hãy tính biến thiên enthalpy của 2 phản ứng sau:
2H2(g) + O2(g) 2H2O(g) (1)
C7H16(g) + 11O2(g) 7CO2(g) + 8H2O(g) (2)
So sánh kết quả thu được, từ đó cho biết H2 hay C7H16 là nhiên liệu hiệu quả hơn cho tên lửa (biết trong C7H16 có 6 liên kết C-C và 16 liên kết C-H)

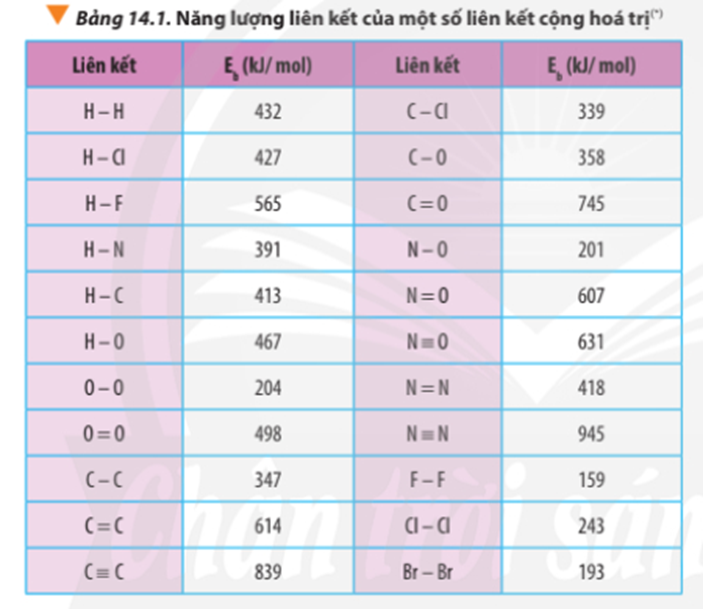
Dựa vào số liệu về năng lượng liên kết ở Bảng 14.1, hãy tính biến thiên enthalpy của 2 phản ứng sau:
2H2(g) + O2(g) 2H2O(g) (1)
C7H16(g) + 11O2(g) 7CO2(g) + 8H2O(g) (2)
So sánh kết quả thu được, từ đó cho biết H2 hay C7H16 là nhiên liệu hiệu quả hơn cho tên lửa (biết trong C7H16 có 6 liên kết C-C và 16 liên kết C-H)


Quảng cáo
Trả lời:
2H2(g) + O2(g) 2H2O(g) (1)
∆ r(1) = 2.Eb(H2) + Eb(O2) – 2.Eb(H2O)
∆ r(1) = 2.Eb(H-H) + Eb(O=O) – 2.2.Eb(O-H)
∆ r(1) = 2.432 + 498 – 2.2.467 = -506 kJ
C7H16(g) + 11O2(g) 7CO2(g) + 8H2O(g) (2)
∆ r(2) = Eb(C7H16) + 11.Eb(O2) – 7.Eb(CO2) – 8.Eb(H2O)
∆ r(2) = 6.Eb(C-C) + 16Eb(C-H) + 11.Eb(O=O) – 7.2.Eb(C=O) – 8.2.Eb(O-H)
∆ r(2) = 6.347 + 16.413 + 11.498 – 7.2.745 – 8.2.467 = -3734 kJ
Ta thấy: ∆ r(2) < ∆ r(1)
Tuy nhiên có còn có
Nếu lấy cùng khối lượng nhiên liệu chứng tỏ hydrogen là một loại khí có nhiệt cháy rất cao.
Thực tế hydrogen là một loại khí có nhiệt cháy cao nhất trong tất cả các nhiên liệu trong thiên nhiên, đã được sử dụng làm nhiên liệu phóng các tàu vũ trụ. Hydrogen là nguồn nhiên liệu an toàn, không gây sự cố cho môi trường, sản phẩm cháy chỉ là nước, được gọi là nhiên liệu sạch, lý tưởng.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
C3H8(g) + 5O2(g) 3CO2(g) + 4H2O(g)
Tính theo nhiệt tạo thành của hợp chất:
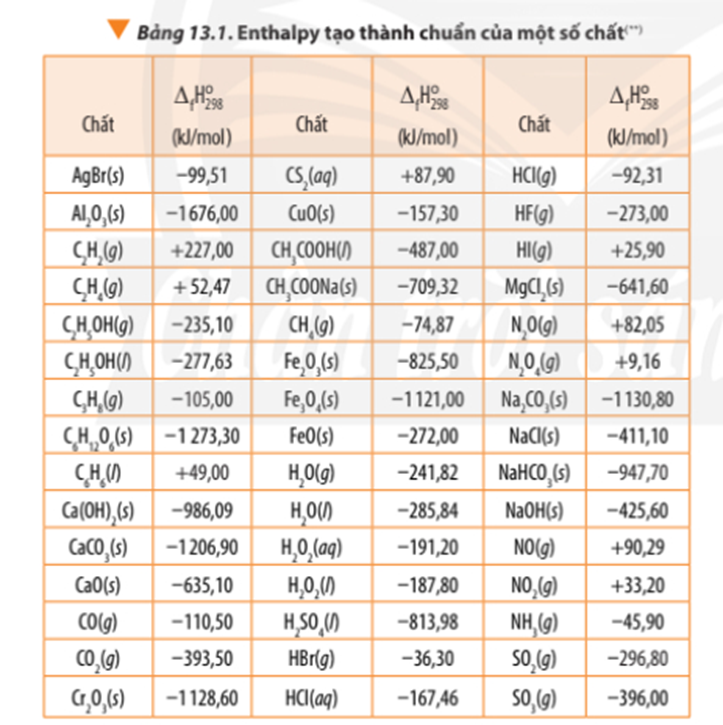
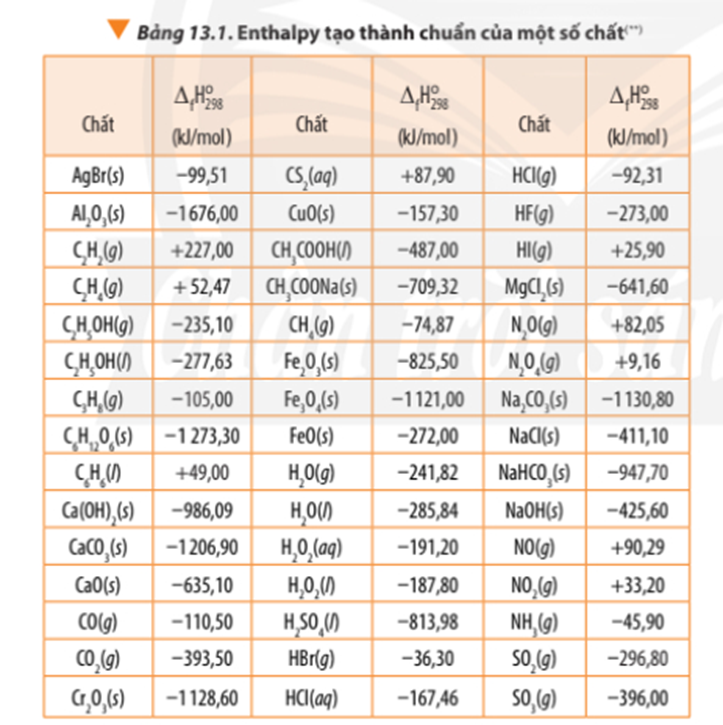
∆ r = 3.∆ f(CO2) + 4. ∆ f(H2O) - ∆ f(C3H8) – 5.∆ f(O2)
∆ r = 3.(-393,50) + 4.(-241,82) – (-105,00) - 5.0
∆ r = -2042,78 kJ
Tính theo năng lượng liên kết:
∆ r = Eb(C3H8) + 5.Eb(O2) – 3Eb(CO2) – 4Eb(H2O)
∆ = 2.Eb(C-C) + 8.Eb(C-H) + 5.Eb(O=O) -3.2.Eb(C=O) - 4.2.Eb(O-H)
∆ r = 2.347 + 8.413 + 5.498 – 3.2.745 – 4.2.467
∆ r = -1718 kJ
Nhận xét: Biến thiên enthalpy chuẩn của phản ứng dựa vào nhiệt tạo thành có giá trị -2 042,78 kJ âm hơn so với biến thiên enthalpy chuẩn của phản ứng dựa vào năng lượng liên kết – 1718 kJ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.