Cho phương trình nhiệt hóa học sau:
SO2(g) + O2(g) SO3(g) ∆ r = -98,5 kJ
a) Tính lượng nhiệt giải phóng ra khi chuyển 74,6 g SO2 thành SO3.
b) Giá trị ∆ r của phản ứng: SO3(g) → SO2(g) + O2(g) là bao nhiêu?
Cho phương trình nhiệt hóa học sau:
SO2(g) + O2(g) SO3(g) ∆ r = -98,5 kJ
a) Tính lượng nhiệt giải phóng ra khi chuyển 74,6 g SO2 thành SO3.
b) Giá trị ∆ r của phản ứng: SO3(g) → SO2(g) + O2(g) là bao nhiêu?
Quảng cáo
Trả lời:
a) 74,6 g SO2 tương ứng với mol SO2
Đốt cháy hoàn toàn 1 mol SO2(g) sinh ra 98,5 kJ nhiệt lượng
⇒ Đốt cháy hoàn toàn mol SO2(g) sinh ra 98,5. = 114,81 kJ nhiệt lượng
b) Lượng nhiệt giải phóng ra khi chuyển 1 mol SO2 thành 1 mol SO3 là 98,5 kJ
⇒ Lượng nhiệt cần cung cấp để phân hủy 1 mol SO3 cũng là 98,5 kJ
⇒ Giá trị ∆ r của phản ứng: SO3(g) → SO2(g) + O2(g) là +98,5 kJ.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
C3H8(g) + 5O2(g) 3CO2(g) + 4H2O(g)
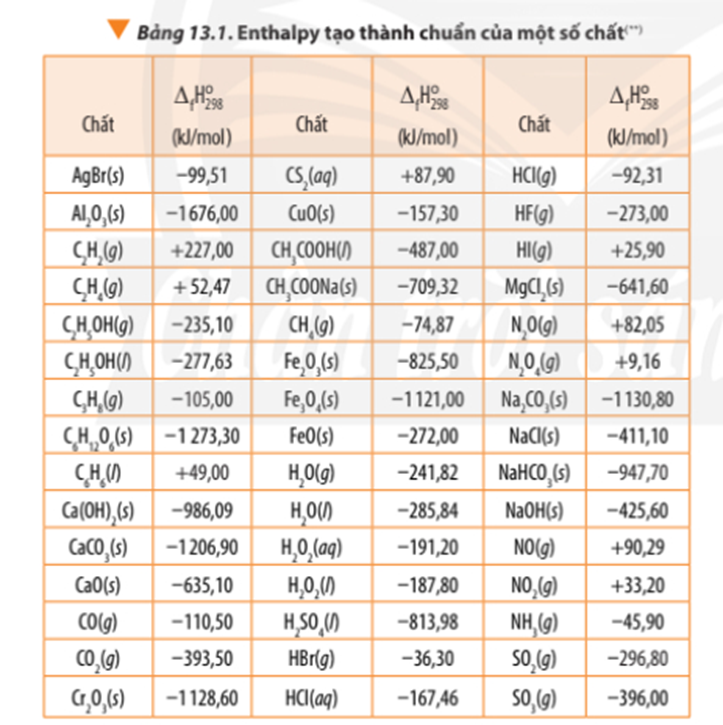
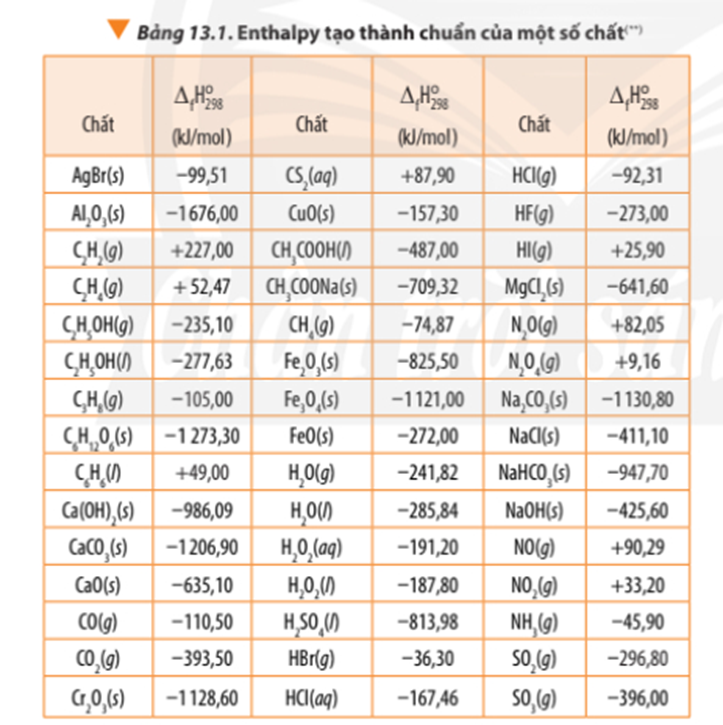
Tính theo nhiệt tạo thành của hợp chất:
∆ r = 3.∆ f(CO2) + 4. ∆ f(H2O) - ∆ f(C3H8) – 5.∆ f(O2)
∆ r = 3.(-393,50) + 4.(-241,82) – (-105,00) - 5.0
∆ r = -2042,78 kJ
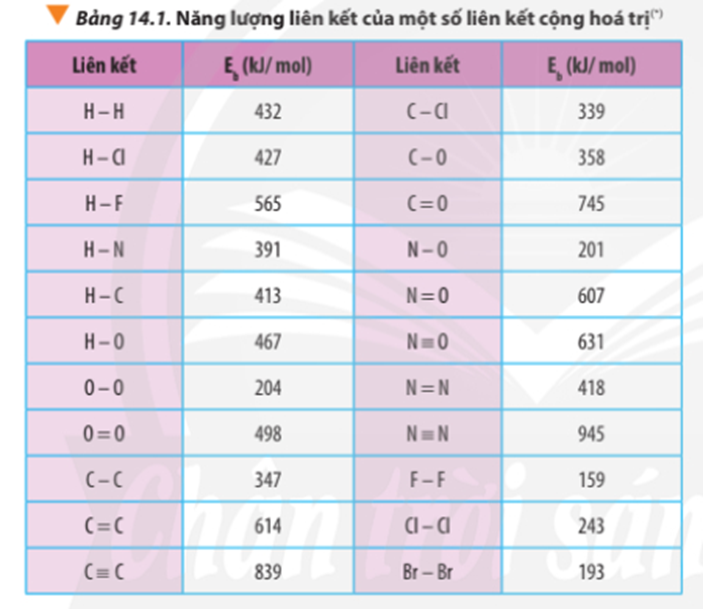
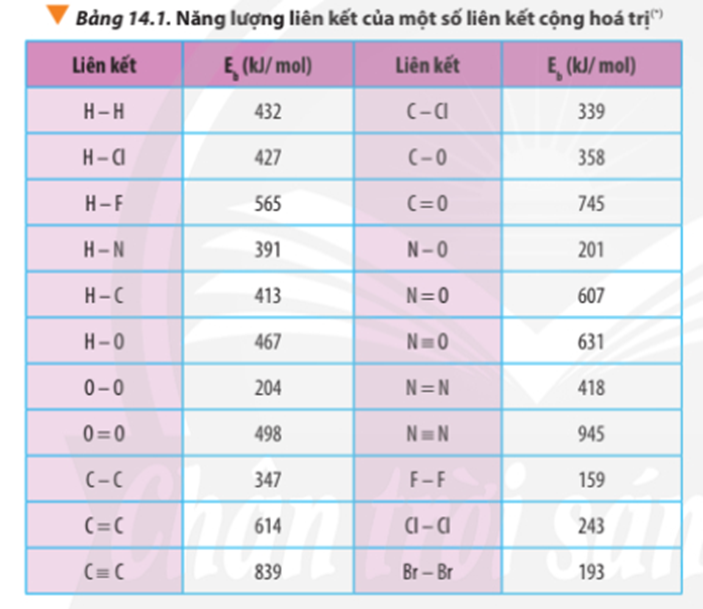
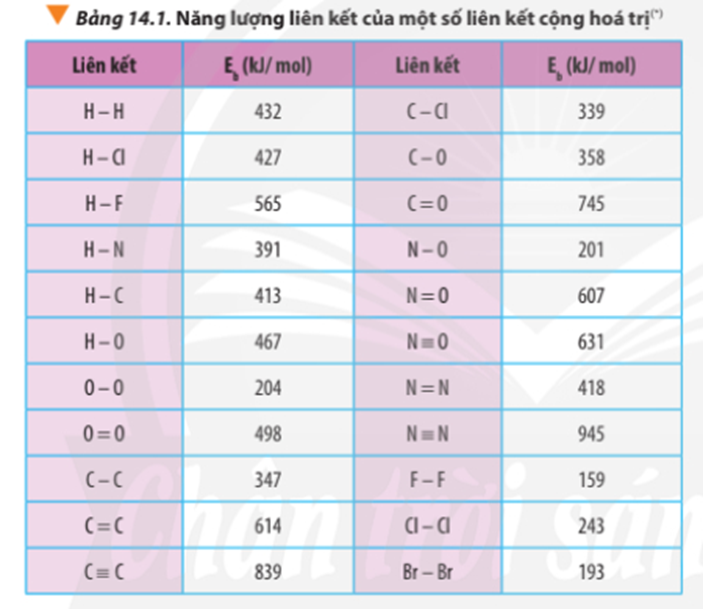
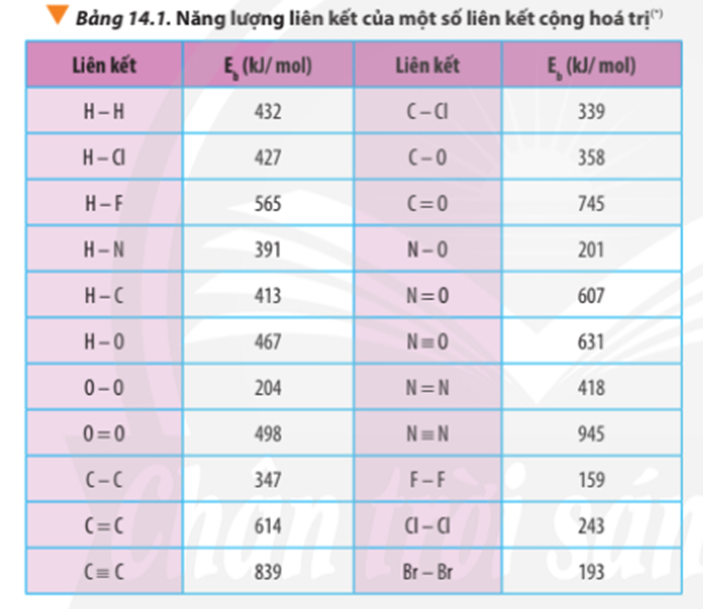
Tính theo năng lượng liên kết:
∆ r = Eb(C3H8) + 5.Eb(O2) – 3Eb(CO2) – 4Eb(H2O)
∆ = 2.Eb(C-C) + 8.Eb(C-H) + 5.Eb(O=O) -3.2.Eb(C=O) - 4.2.Eb(O-H)
∆ r = 2.347 + 8.413 + 5.498 – 3.2.745 – 4.2.467
∆ r = -1718 kJ
Nhận xét: Biến thiên enthalpy chuẩn của phản ứng dựa vào nhiệt tạo thành có giá trị -2 042,78 kJ âm hơn so với biến thiên enthalpy chuẩn của phản ứng dựa vào năng lượng liên kết – 1718 kJ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
























Vàng Nguễn
cứu vớii