Quảng cáo
Trả lời:
Bán kính quỹ đạo thứ nhất của ion He+ là:
Bán kính quỹ đạo thứ nhất của ion Li2+ là:
Bán kính quỹ đạo thứ nhất của ion Be3+ là:
Như vậy, khi điện tích hạt nhân tăng, bán kính quỹ đạo thứ nhất giảm dần. Điều này được giải thích là khi Z tăng, lực hút giữa hạt nhân với electron cũng sẽ tăng nên electron chuyển động về phía gần hạt nhân hơn.
(Lưu ý: Xét cho cùng một lớp).
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án đúng là: A và C
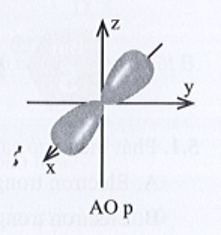
Xác suất tìm thấy electron trong AO p là khoảng 90% nên xác suất tìm thấy electron ở mỗi thùy là khoảng 45%.
Lời giải
Đáp án:
A. chuyển từ lớp electron gần hạt nhân sang lớp xa hạt nhân hơn.
Đáp án đúng là: A
Theo mô hình Rutherford - Bohr, khi một nguyên tử H hấp thụ một năng lượng đủ lớn, electron sẽ chuyển từ lớp electron gần hạt nhân sang lớp xa hạt nhân hơn (hay electron sẽ chuyển từ lớp có năng lượng thấp hơn lên lớp có năng lượng cao hơn).
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.