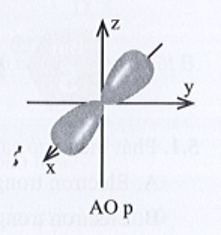
Giải SBT Hóa 10 Bài 4: Mô hình nguyên tử và orbital nguyên tử có đáp án
34 người thi tuần này 4.6 1.2 K lượt thi 16 câu hỏi
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Đề thi cuối kì 2 Hóa học 10 THPT Xuân Hoà (Vĩnh Phúc) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Long Hải - Phước Tỉnh (Bà Rịa - Vũng Tàu) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Kẻ Sặt (Hải Dương) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Kiến Văn (Đồng Tháp) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Gia Lộc (Hải Dương) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Điểu Cải (Đồng Nai) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Sào Nam (Quảng Nam) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Lê Lợi (Quảng Trị) năm 2023-2024 có đáp án
Danh sách câu hỏi:
Lời giải
Đáp án:
A. Số lượng electron tối đa trên các lớp là như nhau.
Đáp án đúng là: C
A sai vì số electron tối đa trên các lớp là khác nhau, ví dụ lớp thứ nhất có tối đa 2 electron; lớp thứ hai có tối đa 8 electron.
B sai vì năng lượng của các electron trên các lớp khác nhau là khác nhau.
D sai vì electron ở gần hạt nhân nhất có năng lượng thấp nhất.
Lời giải
Đáp án:
A. chuyển từ lớp electron gần hạt nhân sang lớp xa hạt nhân hơn.
Đáp án đúng là: A
Theo mô hình Rutherford - Bohr, khi một nguyên tử H hấp thụ một năng lượng đủ lớn, electron sẽ chuyển từ lớp electron gần hạt nhân sang lớp xa hạt nhân hơn (hay electron sẽ chuyển từ lớp có năng lượng thấp hơn lên lớp có năng lượng cao hơn).
Lời giải
Đáp án:
A. Electron trên lớp K có năng lượng cao hơn trên lớp L.
Đáp án đúng là: A
Phát biểu A sai vì: Electron trên lớp K có năng lượng thấp hơn trên lớp L.Lời giải
Đáp án:
A. 2 : 12.
Đáp án đúng là: B
Số lượng electron tối đa trên một lớp là 2.n2 (với n ≤ 4).
Lớp thứ nhất của F chứa tối đa 2 electron.
Lớp thứ hai của F chứa 7 electron (lớp thứ hai tối đa chứa 2.22 = 8 electron).
Vậy tỉ lệ số lượng electron trên lớp thứ hai so với số lượng electron trên lớp thứ nhất là
7 : 2.
Lời giải
Khối lượng nguyên tử tập trung ở (1) hạt nhân. Electron quay xung quanh hạt nhân theo những (2) quỹ đạo xác định. Electron ở càng xa hạt nhân thì có năng lượng càng (3) cao. Khi nguyên tử hấp thụ năng lượng phù hợp, electron sẽ chuyển (4) ra xa hạt nhân hơn.
Lời giải
Đáp án:
A. 2
Đáp án đúng là: A
O có số electron tối đa ở lớp thứ nhất là: 2.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Xem tiếp với tài khoản VIP
Còn 10/16 câu hỏi, đáp án và lời giải chi tiết.
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.