Bài tập Nguyên tố và đơn chất halogen có đáp án
38 người thi tuần này 4.6 1.5 K lượt thi 16 câu hỏi
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Đề thi cuối kì 2 Hóa học 10 THPT Xuân Hoà (Vĩnh Phúc) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Long Hải - Phước Tỉnh (Bà Rịa - Vũng Tàu) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Kẻ Sặt (Hải Dương) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Kiến Văn (Đồng Tháp) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Gia Lộc (Hải Dương) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Điểu Cải (Đồng Nai) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Sào Nam (Quảng Nam) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Lê Lợi (Quảng Trị) năm 2023-2024 có đáp án
Danh sách câu hỏi:
Lời giải
Khi cho chlorine vào nước sẽ xảy ra phản ứng:
Cl2(aq) + H2O(l) ⇄ HCl(aq) + HClO(aq)
Phản ứng này là thuận nghịch nên tạo ra dung dịch gồm: nước, hydrochloric acid (HCl), hypochlorous acid (HClO còn được viết là HOCl) và chlorine. Dung dịch này còn được gọi là dung dịch nước chlorine, có tính sát khuẩn. Vì vậy, nước chlorine được sử dụng phổ biến để khử trùng, sát khuẩn trong các nguồn nước cấp, môi trường
Lời giải
Khi phân tử halogen có kích thước càng lớn và càng nhiều electron thì mức độ chuyển động hỗn loạn của các electron càng cao. Vì vậy thường xuyên có sự phân bố không đồng đều các electron tại một thời điểm nào đó, dễ làm xuất hiện các lưỡng cực tạm thời ở mỗi phân tử. Điều này sẽ làm tăng tương tác van der Waals giữa các phân tử halogen với nhau hay nói cách khác các phân tử halogen tương tác với nhau chặt chẽ hơn.
Trong nhóm VIIA, theo chiều tăng dần điện tích hạt nhân nguyên tử, khối lượng nguyên tử có xu hướng tăng ⇒ Khối lượng phân tử halogen X2 có xu hướng tăng ⇒ Sự tương tác giữa các phân tử trong mỗi halogen X2 tăng.
Dựa vào bảng 17.3 ta có thể thấy thể của các halogen ở điều kiện thường biến đổi từ khí (fluorine, chlorine) đến lỏng (bromine) và rắn (iodine). Mà astatine có khối lượng phân tử lớn hơn iodine.
Vậy ta có thể dự đoán đơn chất astatine tồn tại ở thể rắn ở điều kiện thường.
Lời giải
Dựa theo xu hướng tăng khối lượng phân tử và sự tương tác giữa các phân tử.
Khi phân tử X2 có kích thước càng lớn và càng nhiều electron thì tương tác van der Waals giữa các phân tử càng mạnh. Do đó, trong các halogen, tương tác tăng từ fluorine đến iodine.
Ở điều kiện thường bắt đầu từ iodine (I) tồn tại ở thể rắn, các nguyên tố có khối lượng phân tử lớn hơn iodine (I) là astatine At, tennessine (Ts) cũng ở thể rắn
Lời giải
Theo quy tắc octet:
Ca (Z = 20): [Ar]4s2 có xu hướng nhường 2 electron.
F (Z = 9): [He]2s22p5 có xu hướng nhận 1 electron
Khi calcium và fluorine kết hợp thành phân tử calcium fluoride (CaF2) có sự nhận và nhường electron như sau:
- Mỗi nguyên tử F nhận thêm 1 electron từ nguyên tử Ca tạo thành anion F-
⇒ Phân tử F2 gồm 2 nguyên tử F nhận tổng cộng 2 electron từ nguyên tử Ca
F2 + 2e → 2F‑
- Đồng thời nguyên tử Ca đã nhường 2 electron để trở thành cation Ca2+
Ca → Ca2+ + 2e
- Giữa anion và cation hút nhau bằng lực hút tĩnh điện để tạo thành phân tử calcium fluoride (CaF2).
Phương trình hóa học của phản ứng là:
Ca + F2 → CaF2
Lời giải
Theo quy tắc octet:
P (Z = 15): [Ne]2s22p3 có 5 electron lớp ngoài cùng. Thiếu 3 electron để đạt được cấu hình electron bền vững.
Cl (Z = 17): [Ne]2s22p5 có 7 electron lớp ngoài cùng. Thiếu 1 electron để đạt được cấu hình electron bền vững.
Để đạt được cấu hình của khí hiếm gần nhất, mỗi nguyên tử Cl đều cần thêm 1 electron. Vì vậy, nguyên tử P sẽ góp chung 3 electron với 3 nguyên tử Cl để tạo nên 3 cặp electron chung cho cả hai nguyên tử.
Công thức Lewis của phân tử:
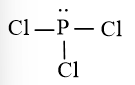
Lời giải
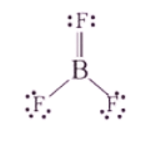
a) Phương trình hóa học:
2B + 3F2 → 2BF3
b) Phân tử BF3 gồm 2 liên kết σ và 1 liên kết π.
Câu 7/16
Theo dõi mô tả thí nghiệm chlorine phản ứng với hydrogen như dưới đây.
Hoặc quan sát video thí nghiệm theo đường link sau:
https://www.youtube.com/wach?v=esGk1lh1Nds, truy cập ngày 30/3/2022.
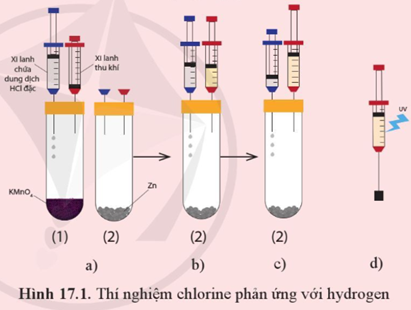
- Các dụng cụ thí nghiệm được mô tả như Hình 17.1a với các ống nghiệm cùng đặt vào một giá thí nghiệm.
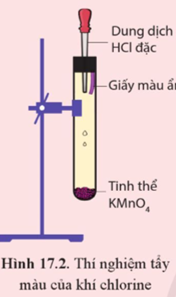
- Bơm vài giọt dung dịch hydrochloric acid (HCl) đặc từ xilanh chứa acid vào ống nghiệm chứa tinh thể potassium permanganate (thuốc tím, KMnO4) - ống nghiệm (1) để tạo khí chlorine. Khi pit-tông nâng lên khoảng chiều cao của xi-lanh thu khí thì ngừng bơm acid (hình 17.1b)
- Rút xi-lanh thu khí ra khỏi ống nghiệm (1), chuyển sang ghim vào ống nghiệm chứa kẽm - ống nghiệm (2). Chuyển xi-lanh chứa dung dịch hydrochloric acid sang ống nghiệm (2). (Hình 17.1b)
- Bơm vài giọt dung dịch hydrochloric acid từ xi-lanh chứa acid vào ống nghiệm (2) để tạo khí hydrogen. Đến khi pit-tông được nâng lên khoảng xi-lanh thu khí thì ngừng bơm acid. (Hình 17.1c)
- Rút xi-lanh thu khí ra khỏi ống nghiệm (2). Ghim xi-lanh chứa hỗn hợp khí vào một nút cao su như hình 17.1d rồi kẹp vào giá thí nghiệm.
- Dùng đèn tử ngoại chiếu vào xi-lanh chứa hỗn hợp khí (hoặc dùng ngọn lửa hơ nhẹ bên ngoài xi-lanh.
+ Quan sát và giải thích hiện tượng xảy ra khi dùng đèn tử ngoại chiếu vào xi-lanh chứa hỗn hợp khí (hoặc dùng ngọn lửa hơ nhẹ bên ngoài xi-lanh)
+ Nếu thay khí chlorine bằng hơi iodine thì phản ứng giữa hơi iodine và hydrogen có thể xảy ra hiện tượng như đã thấy trong thí nghiệm trên không? Giải thích.
Theo dõi mô tả thí nghiệm chlorine phản ứng với hydrogen như dưới đây.
Hoặc quan sát video thí nghiệm theo đường link sau:
https://www.youtube.com/wach?v=esGk1lh1Nds, truy cập ngày 30/3/2022.
- Các dụng cụ thí nghiệm được mô tả như Hình 17.1a với các ống nghiệm cùng đặt vào một giá thí nghiệm.
- Bơm vài giọt dung dịch hydrochloric acid (HCl) đặc từ xilanh chứa acid vào ống nghiệm chứa tinh thể potassium permanganate (thuốc tím, KMnO4) - ống nghiệm (1) để tạo khí chlorine. Khi pit-tông nâng lên khoảng chiều cao của xi-lanh thu khí thì ngừng bơm acid (hình 17.1b)
- Rút xi-lanh thu khí ra khỏi ống nghiệm (1), chuyển sang ghim vào ống nghiệm chứa kẽm - ống nghiệm (2). Chuyển xi-lanh chứa dung dịch hydrochloric acid sang ống nghiệm (2). (Hình 17.1b)
- Bơm vài giọt dung dịch hydrochloric acid từ xi-lanh chứa acid vào ống nghiệm (2) để tạo khí hydrogen. Đến khi pit-tông được nâng lên khoảng xi-lanh thu khí thì ngừng bơm acid. (Hình 17.1c)
- Rút xi-lanh thu khí ra khỏi ống nghiệm (2). Ghim xi-lanh chứa hỗn hợp khí vào một nút cao su như hình 17.1d rồi kẹp vào giá thí nghiệm.
- Dùng đèn tử ngoại chiếu vào xi-lanh chứa hỗn hợp khí (hoặc dùng ngọn lửa hơ nhẹ bên ngoài xi-lanh.
+ Quan sát và giải thích hiện tượng xảy ra khi dùng đèn tử ngoại chiếu vào xi-lanh chứa hỗn hợp khí (hoặc dùng ngọn lửa hơ nhẹ bên ngoài xi-lanh)
+ Nếu thay khí chlorine bằng hơi iodine thì phản ứng giữa hơi iodine và hydrogen có thể xảy ra hiện tượng như đã thấy trong thí nghiệm trên không? Giải thích.

Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Xem tiếp với tài khoản VIP
Còn 10/16 câu hỏi, đáp án và lời giải chi tiết.
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.