Xét phân tử H2O, những phát biểu nào sau đây là đúng?
A. Liên kết H – O là liên kết cộng hoá trị không phân cực.
B. Liên kết H – O là liên kết cộng hoá trị phân cực.
C. Cặp electron dùng chung trong liên kết H – O lệch về phía nguyên tử O.
D. Cặp electron dùng chung trong liên kết H – O lệch về phía nguyên tử H.
E. Cặp electron dùng chung trong liên kết H – O phân bố đều giữa hai nguyên tử.
G. Nguyên tử O còn hai cặp electron hoá trị riêng.
Xét phân tử H2O, những phát biểu nào sau đây là đúng?
A. Liên kết H – O là liên kết cộng hoá trị không phân cực.
B. Liên kết H – O là liên kết cộng hoá trị phân cực.
C. Cặp electron dùng chung trong liên kết H – O lệch về phía nguyên tử O.
D. Cặp electron dùng chung trong liên kết H – O lệch về phía nguyên tử H.
E. Cặp electron dùng chung trong liên kết H – O phân bố đều giữa hai nguyên tử.
G. Nguyên tử O còn hai cặp electron hoá trị riêng.
Câu hỏi trong đề: Giải SBT Hóa 10 Bài 11: Liên kết cộng hóa trị có đáp án !!
Quảng cáo
Trả lời:
Đáp án đúng là: B, C, G.
- Liên kết H – O trong phân tử nước là liên kết cộng hóa trị phân cực, cặp electron chung bị lệch về phía nguyên tử có độ âm điện cao hơn là O.
- Công thức Lewis của H2O là:
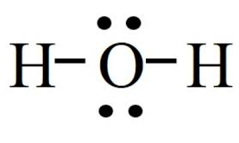
Vậy nguyên tử O còn hai cặp electron hóa trị riêng.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án:
A. 1, 2, 3, 4.
Đáp án đúng là: B
+ Nguyên tử H có 1 electron ở lớp ngoài cùng, mỗi nguyên tử H có xu hướng góp chung 1 electron để tạo thành phân tử H2. Công thức cấu tạo: H – H.
+ Nguyên tử O có 6 electron ở lớp ngoài cùng, mỗi nguyên tử O có xu hướng góp chung 2 electron để tạo thành phân tử O2. Công thức cấu tạo: O = O.
+ Nguyên tử N có 5 electron ở lớp ngoài cùng, mỗi nguyên tử N có xu hướng góp chung 3 electron để tạo thành phân tử N2. Công thức cấu tạo: N ≡ N.
+ Nguyên tử F có 7 electron ở lớp ngoài cùng, mỗi nguyên tử F có xu hướng góp chung 1 electron để tạo thành phân tử F2. Công thức cấu tạo: F – F.
Số lượng cặp electron dùng chung trong các phân tử H2, O2, N2, F2 lần lượt là: 1, 2, 3, 1.
Lời giải
Đáp án:
A. Phân lớp 2s, hình cầu.
Đáp án đúng là: C
Cấu hình electron của F: 1s22s22p5.
Khi tham gia hình thành liên kết trong các phân tử HF, F2; orbital tham gia xen phủ tạo liên kết của nguyên tử F thuộc về phân lớp 2p.
AO p có dạng số tám nổi.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















