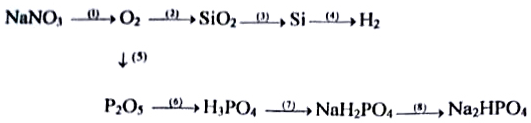Giải thích vì sao không dùng bình chữa cháy chứa khí CO2 để dập tắc các đám cháy than hay kim loại đứng trước Zn?
Giải thích vì sao không dùng bình chữa cháy chứa khí CO2 để dập tắc các đám cháy than hay kim loại đứng trước Zn?
Câu hỏi trong đề: Bộ 30 đề thi học kì 1 Hóa 11 có đáp án !!
Quảng cáo
Trả lời:
Phương pháp giải:
Kim loại có tính khử mạnh như Mg, Al,… có thể cháy được trong khí CO2.
Giải chi tiết:
Kim loại có tính khử mạnh (thí dụ Mg, Al,…) có thể cháy được trong khí CO2:
Vì vậy, người ta không dùng khí CO2 để dập tắt đám cháy magie hoặc nhôm.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Phương pháp giải:
- Sử dụng dung dịch NaOH, nhận biết được dung dịch NH4Cl
- Sử dụng axit HCl nhận biết được các chất còn lại
Giải chi tiết:
- Trích các mẫu nhận biết vào các ống nghiệm.
- Nhỏ vài giọt dung dịch NaOH vào các ống nghiệm
+ Xuất hiện khí không màu, mùi khai: NH4Cl
+ Không có hiện tượng: Na2CO3, Na2SiO3, Na3PO4
PTHH:
- Nhỏ vài giọt dung dịch HCl vào các ống nghiệm chưa được nhận biết
+ Có khí không màu thoát ra: Na2CO3
+ Xuất hiện kết tủa keo: Na2SiO3
+ Không có hiện tượng: Na3PO4
PTHH:
Lời giải
Phương pháp giải:
- Gọi số mol O2 là x, suy ra số mol của NO2 theo số mol O2
- Áp dụng bảo toàn khối lượng, tìm ra số mol O2
- Viết phương trình phản ứng của hỗn hợp X với nước
- Tính số mol HNO3 theo số mol O2
- Tính số mol H+
- Tính nồng độ H+
- Tính pH của dung dịch thu được.
Giải chi tiết:
PTHH:
Gọi số mol O2 là x → số mol của NO2 là 4x
Áp dụng bảo toàn khối lượng cho phản ứng:
Dẫn hỗn hợp khí X vào nước ta có phương trình:
Theo phương trình,
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.