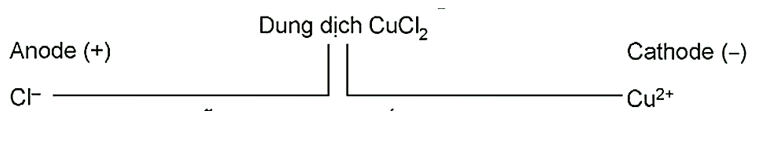
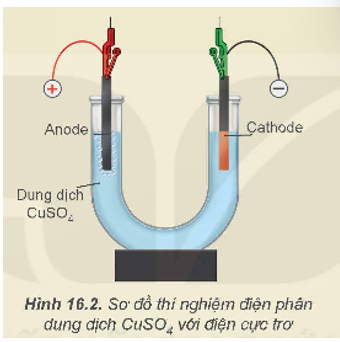
Thí nghiệm: Điện phân dung dịch NaCl (tự điều chế nước Javel để tẩy rửa)
Chuẩn bị:
Hoá chất: dung dịch NaCl bão hoà, cánh hoa màu hồng.
Dụng cụ: nguồn điện một chiều (3 – 6 vôn), cốc thuỷ tinh 100 mL, hai điện cực than chì, dây dẫn, kẹp kim loại.
Tiến hành:
- Lắp thiết bị thí nghiệm điện phân dung dịch NaCl với điện cực trơ như Hình 16.3.
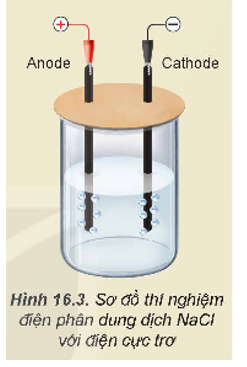
- Rót khoảng 80 mL dung dịch NaCl bão hoà vào cốc rồi nhúng hai điện cực than chì vào dung dịch.
- Nối hai điện cực than chì với hai cực của nguồn điện và tiến hành điện phân trong khoảng 5 phút.
- Cho một mẩu cánh hoa màu hồng vào cốc chứa khoảng 5 mL dung dịch sau điện phân.
Quan sát hiện tượng xảy ra và thực hiện các yêu cầu sau:
1. Giải thích hiện tượng quan sát được ở mỗi điện cực.
2. Giải thích khả năng tẩy màu của dung dịch sau điện phân.
3. Tại sao nên dùng nắp đậy trong quá trình điện phân?
Thí nghiệm: Điện phân dung dịch NaCl (tự điều chế nước Javel để tẩy rửa)
Chuẩn bị:
Hoá chất: dung dịch NaCl bão hoà, cánh hoa màu hồng.
Dụng cụ: nguồn điện một chiều (3 – 6 vôn), cốc thuỷ tinh 100 mL, hai điện cực than chì, dây dẫn, kẹp kim loại.
Tiến hành:
- Lắp thiết bị thí nghiệm điện phân dung dịch NaCl với điện cực trơ như Hình 16.3.

- Rót khoảng 80 mL dung dịch NaCl bão hoà vào cốc rồi nhúng hai điện cực than chì vào dung dịch.
- Nối hai điện cực than chì với hai cực của nguồn điện và tiến hành điện phân trong khoảng 5 phút.
- Cho một mẩu cánh hoa màu hồng vào cốc chứa khoảng 5 mL dung dịch sau điện phân.
Quan sát hiện tượng xảy ra và thực hiện các yêu cầu sau:
1. Giải thích hiện tượng quan sát được ở mỗi điện cực.
2. Giải thích khả năng tẩy màu của dung dịch sau điện phân.
3. Tại sao nên dùng nắp đậy trong quá trình điện phân?
Câu hỏi trong đề: Giải SGK Hoá học 12 Cánh Diều Bài 16: Điện phân có đáp án !!
Quảng cáo
Trả lời:
1. Hiện tượng: Ở hai điện cực đều có khí thoát ra.
Giải thích:
Quá trình oxi hoá, quá trình khử xảy ra ở mỗi điện cực:
Tại anode:
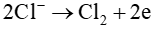
Tại cathode:
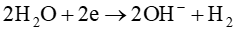
2. Dung dịch sau điện phân có tính tẩy màu, do không có màng ngăn giữa 2 cực nên sản phẩm tạo thành ở hai điện cực khuếch tán vào nhau sẽ xảy ra phản ứng hoá học tạo thành nước Javel:
Cl2 + 2NaOH → NaCl + NaClO + H2O
NaClO có tính oxi hoá mạnh, có khả năng phá huỷ các hợp chất màu (tính tẩy màu).
3. Nên dùng nắp đậy trong quá trình điện phân để tăng hiệu suất điều chế nước Javel, đồng thời hạn chế sự thoát Cl2 ra ngoài môi trường gây độc hại cho người làm thí nghiệm và ô nhiễm môi trường.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Tại anode (cực dương):
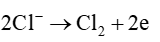
Tại cathode (cực âm):
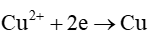
Phương trình hoá học của phản ứng điện phân:
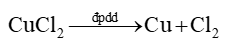
Lời giải
a) Quá trình oxi hoá, quá trình khử xảy ra ở mỗi điện cực:
Tại anode:
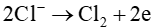
Tại cathode:
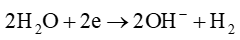
b) Phương trình hoá học của phản ứng điện phân:
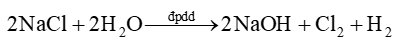
c) Trong quá trình điện phân, sản phẩm tạo thành ở hai điện cực khuếch tán vào nhau sẽ xảy ra phản ứng hoá học tạo thành nước Javel:
Cl2 + 2NaOH → NaCl + NaClO + H2O
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
Quá trình điện phân NaCl nóng chảy được tiến hành theo hai bước như sau:
Bước 1: Nung NaCl trong bình đến nóng chảy, thu được chất lỏng có khả năng dẫn điện.
Bước 2: Nhúng hai điện cực than chì vào bình đựng NaCl nóng chảy rồi nối chúng với hai cực của nguồn điện một chiều (khoảng 7 V). Các ion di chuyển về các điện cực trái dấu, ở điện cực dương có khí Cl2 thoát ra và ở điện cực âm, Na được tạo thành.
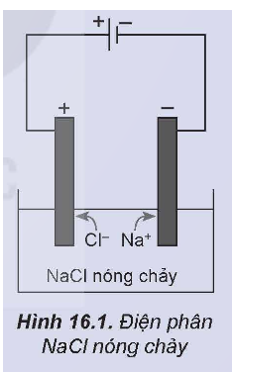
Thực hiện các yêu cầu sau:
1. Viết phương trình phân li của NaCl ở bước 1.
2. Viết quá trình xảy ra ở mỗi điện cực.
3. Viết phương trình hoá học của phản ứng xảy ra trong quá trình điện phân.
Quá trình điện phân NaCl nóng chảy được tiến hành theo hai bước như sau:
Bước 1: Nung NaCl trong bình đến nóng chảy, thu được chất lỏng có khả năng dẫn điện.
Bước 2: Nhúng hai điện cực than chì vào bình đựng NaCl nóng chảy rồi nối chúng với hai cực của nguồn điện một chiều (khoảng 7 V). Các ion di chuyển về các điện cực trái dấu, ở điện cực dương có khí Cl2 thoát ra và ở điện cực âm, Na được tạo thành.

Thực hiện các yêu cầu sau:
1. Viết phương trình phân li của NaCl ở bước 1.
2. Viết quá trình xảy ra ở mỗi điện cực.
3. Viết phương trình hoá học của phản ứng xảy ra trong quá trình điện phân.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.