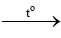
Một số đại lượng đặc trưng của các nguyên tố nhóm IA được trình bày trong Bảng 24.1:
Thực hiện các yêu cầu sau:
1. Nhận xét về xu hướng biến đổi bán kính nguyên tử của nguyên tố nhóm IA.
2. Cho biết: xu hướng biến đổi tính khử từ Li đến Cs; số oxi hoá đặc trưng của nguyên tử kim loại nhóm IA.
Một số đại lượng đặc trưng của các nguyên tố nhóm IA được trình bày trong Bảng 24.1:

Thực hiện các yêu cầu sau:
1. Nhận xét về xu hướng biến đổi bán kính nguyên tử của nguyên tố nhóm IA.
2. Cho biết: xu hướng biến đổi tính khử từ Li đến Cs; số oxi hoá đặc trưng của nguyên tử kim loại nhóm IA.
Quảng cáo
Trả lời:
1. Trong nhóm IA, theo chiều từ trên xuống dưới (chiều tăng dần của điện tích hạt nhân) bán kính nguyên tử tăng dần.
2. Dựa vào thế điện cực chuẩn xác định được từ Li đến Cs tính khử của kim loại tăng dần;
Do nguyên tố nhóm IA là những nguyên tố s, chỉ có 1 electron hoá trị ở phân lớp ns1 nên số oxi hoá đặc trưng của nguyên tử kim loại nhóm IA trong hợp chất là +1.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Trong dung dịch:
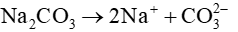
Phương trình hoá học để giải thích các ứng dụng:
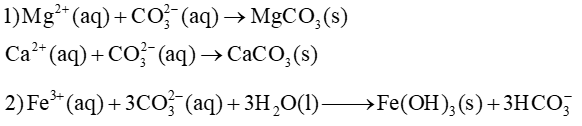
Lời giải
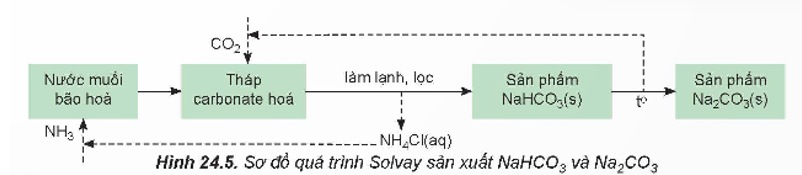
a) Trong quá trình Solvay viết các phương trình hoá học của phản ứng:
- Nung vôi để cung cấp vôi sống và carbon dioxide:
CaCO3 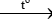 CaO + CO2
CaO + CO2
- Tái chế ammonia từ vôi sống và dung dịch ammonium chloride.
CaO + H2O → Ca(OH)2
Ca(OH)2 + 2NH4Cl → CaCl2 + 2NH3↑ + 2H2O
Hoặc có thể viết gọn:
2NH4Cl + CaO → 2NH3 + CaCl2 + H2O
b) Quy trình Solvay đã giảm thiểu được tác động đến môi trường bằng cách quay vòng các sản phẩm trung gian (như CO2 và NH3) để tái sử dụng trong quy trình sản xuất.
Từ sơ đồ quá trình Solvay, ta có quá trình cụ thể như sau:
(1) Hoà tan NaCl vào dung dịch NH3 đặc đến bão hoà.
(2) Nung CaCO3, rồi dẫn khí thoát ra vào dung dịch bão hoà của NaCl trong NH3:
CaCO3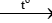 CaO + CO2
CaO + CO2
NaCl + NH3 + CO2 + H2O 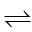 NaHCO3 + NH4Cl
NaHCO3 + NH4Cl
(3) Do NaHCO3 ít tan hơn các muối khác nên kết tinh trước. Tách NaHCO3 ra khỏi dung dịch, nung ở nhiệt độ cao được soda:
2NaHCO3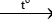 Na2CO3 + CO2 + H2O
Na2CO3 + CO2 + H2O
(4) Sản phẩm NH4Cl được chế hoá bởi vôi tôi, thu khí NH3:
2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3 + 2H2O
Các khí CO2, NH3 được đưa vào sử dụng lại. NH3 được tuần hoàn trong quá trình sản xuất.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.