Viết các cặp oxi hoá – khử trong quá trình (2) và (3).
Ví dụ 1:
Cu2+ + 2e ⇌ Cu (2)
Ag+ + 1e ⇌ Ag (3)
Viết các cặp oxi hoá – khử trong quá trình (2) và (3).
Ví dụ 1:
Cu2+ + 2e ⇌ Cu (2)
Ag+ + 1e ⇌ Ag (3)
Quảng cáo
Trả lời:
- Quá trình (2): Cu2+ + 2e ⇌ Cu
Cặp oxi hoá – khử: Cu2+/Cu.
- Quá trình (3): Ag+ + 1e ⇌ Ag
Cặp oxi hoá – khử: Ag+/Ag.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án đúng là: A
Phản ứng oxi hoá – khử diễn ra trong pin:
Fe + 2Ag+ → Fe2+ + 2Ag
Trong pin điện hoá, cực âm là anode, xảy ra quá trình nhường electron.
Vậy, quá trình xảy ra ở cực âm khi pin hoạt động là: Fe → Fe2+ + 2e.
Lời giải
Đáp án đúng là: A
Phản ứng oxi hoá – khử xảy ra trong pin:
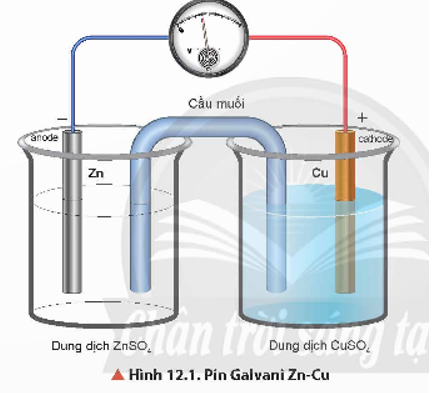
Zn + Cu2+ → Zn2+ + Cu
Vậy, khi pin Galvani Zn-Cu hoạt động thì nồng độ Cu2+ giảm, Zn2+ tăng.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.