Có ba chai thuỷ tinh giống nhau (khối lượng và dung tích bằng nhau) đựng các chất khí khác nhau (He, C4H10, CO2) ở cùng nhiệt độ 20 °C và áp suất 1,913.105 Pa. Các chai đựng khí được cân bằng cân điện tử. Kết quả cân được ghi trong hàng thứ 2 bảng dưới.
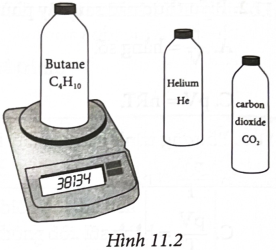
1. Tính các giá trị còn trống trong bảng, biết khối lượng của chai khi chưa chứa khí là 378,68 g
2. So sánh các số liệu tìm được trong hàng cuối. Có phải chúng ta có thể dự đoán được kết quả so sánh này không? Tại sao?
3. Hãy dùng phương trình trạng thái của khí lí tưởng để tìm lại các giá trị của n trong bảng.
Khí
He
C4H10
CO2
Kết quả cân (g)
378,86
381,34
380,70
Khối lượng khí m (g)
Khối lượng mol M (g/mol)
Số mol n
Có ba chai thuỷ tinh giống nhau (khối lượng và dung tích bằng nhau) đựng các chất khí khác nhau (He, C4H10, CO2) ở cùng nhiệt độ 20 °C và áp suất 1,913.105 Pa. Các chai đựng khí được cân bằng cân điện tử. Kết quả cân được ghi trong hàng thứ 2 bảng dưới.

1. Tính các giá trị còn trống trong bảng, biết khối lượng của chai khi chưa chứa khí là 378,68 g
2. So sánh các số liệu tìm được trong hàng cuối. Có phải chúng ta có thể dự đoán được kết quả so sánh này không? Tại sao?
3. Hãy dùng phương trình trạng thái của khí lí tưởng để tìm lại các giá trị của n trong bảng.
|
Khí |
He |
C4H10 |
CO2 |
|
Kết quả cân (g) |
378,86 |
381,34 |
380,70 |
|
Khối lượng khí m (g) |
|
|
|
|
Khối lượng mol M (g/mol) |
|
|
|
|
Số mol n |
|
|
|
Quảng cáo
Trả lời:
1.
|
Khí |
He |
C4H10 |
CO2 |
|
Kết quả cân (g) |
378,86 |
381,34 |
380,70 |
|
Khối lượng khí m (g) |
0,18 |
2,66 |
2,02 |
|
Khối lượng mol M (g/mol) |
4 |
58 |
44 |
|
Số mol n |
0,045 |
0,045 |
0,045 |
2. Số mol trong các chai bằng nhau. Có thể tiên đoán được dựa trên phương trình: pV = nRT
3. Hướng dẫn cách làm. Ví dụ với chai chứa CO2.
- Dựa vào thể tích của 1 mol khí CO2 ở điều kiện chuẩn để xác định thể tích của một mol khí CO2 ở điều kiện (T = 293 K và p = 1,913.105 Pa), từ đó suy ra thể tích của 2,02 g khí CO2 ở điều kiện (T = 293 K và p = 1,913.105 Pa).
- Áp dụng phương trình pV = nRT cho khí CO2 với các dữ liệu (V = 0,58 lít = 0,58.10-3 m3); T = 293 K; p = 1,913.105 Pa và R = 8,31 để tính n.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
– Xác định độ lớn của áp suất ở độ sâu 100 m:
p2 = pkhí quyển + pnước = 1,013.105 + (1 000. 9,81.100) = 10,82.105 Pa.
– Xác định trạng thái của lượng khí khi chưa giãn nở (V1 = 60 lít; p1 = 107 Pa; T1 = 300 K) và khi đã giãn nở (V2 = ?; T2 = 276 K; p2 = 10,82.105 Pa). Từ đó tính được V2 = 510 lít.
Lời giải
T0 = 279 K và p0 = 1,00 bar = 105 Pa; T = T1 = 300 K
1. Lượng không khí trong khí cầu khi chưa bay lên:
Khối lượng không khí trong khí cầu khi chưa bay lên: mkk = n.MA = 1,16.103 kg.
Khối lượng của cả khí cầu: mkc = 240 kg + 1,16.103 kg = 1,40.103 kg.
2. Trạng thái của không khí trong khí cầu khi chưa bay lên:
Trạng thái của không khí trong khí cầu khi bay lên:
Coi khi bay lên lực đẩy Archimedes bằng trọng lượng của khí cầu:
(1)
Từ phương trình trạng thái của khí lí tưởng: và công thức tính khối lượng riêng của không khí: rút ra:
Từ (1) suy ra
3. Vì số mol n và áp suất p của không khí trong khí cầu không đổi nên đây là quá trình đẳng áp của một lượng khí không đổi:
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
A. Không khí bị đun nóng trong một bình kín.
C. Không khí trong một quả bóng bay bị em bé bóp bẹp.
D. Cả ba hiện tượng trên.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















