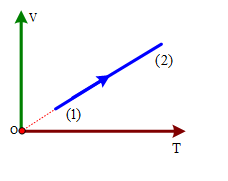
Có 20 g khí Helium chứa trong xilanh đậy kín bởi 1 pittong biến đổi chậm từ trạng thái (1) đến trạng thái (2) theo đồ thị như hình vẽ. Cho V1 = 30,0 lít, p1 = 5,00 atm, V2 = 10,0 lít, p2 = 15,0 atm. Nhiệt độ cao nhất mà khí đạt được trong quá trình trên là bao nhiêu K? Cho khối lượng mol của Helium là 4 g/mol. (làm tròn kết quả đến chữ số hàng đơn vị).
Có 20 g khí Helium chứa trong xilanh đậy kín bởi 1 pittong biến đổi chậm từ trạng thái (1) đến trạng thái (2) theo đồ thị như hình vẽ. Cho V1 = 30,0 lít, p1 = 5,00 atm, V2 = 10,0 lít, p2 = 15,0 atm. Nhiệt độ cao nhất mà khí đạt được trong quá trình trên là bao nhiêu K? Cho khối lượng mol của Helium là 4 g/mol. (làm tròn kết quả đến chữ số hàng đơn vị).
Quảng cáo
Trả lời:
Quá trình từ trạng thái (1) đến trạng thái (2):
Mà
Suy ra để nhiệt độ của khí cao nhất
Đáp số: 488
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
Lời giải
Chọn đáp án B
Lời giải:
A. sai. Đẳng quá trình phải có đại lượng không đổi, (đẳng quá trình thay đổi một cái gì đó, giữ nguyên một cái gì đó)
B. đúng.
Ví dụ: Đẳng nhiệt giữ cho nhiệt độ không đổi, áp suất và thể tích thay đổi
Đẳng áp là áp suất không đổi, nhiệt độ và thể tích sẽ thay đổi
C. sai
D. sai
Câu 2
Lời giải
Chọn đáp án B
? Lời giải:
Cơ chế giải phóng hơi nước → là van điều chỉnh áp suất để xả bớt lượng khí ra
Xả bớt lượng khí ra (Vì V là hằng số, vì nối áp suất là 1 cái khuân đúc lên áp suất không đổi)
Câu 3
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.