M là muối ngậm nước của sắt có công thức FeC2O4.xH2O. Để xác định x người ta chuẩn độ bằng dung dịch KMnO4 trong môi trường acid H2SO4 loãng và được đun nóng đến 70oC. Lấy 2,6235 gam M hoà tan vào acid H2SO4 loãng và cho thêm nước vào để được 250 mL dung dịch. Lấy 25,00 mL dung dịch này đem chuẩn độ bằng dung dịch KMnO4 0,020 M. Kết quả trung bình của 3 lần chuẩn độ cho thấy thể tích KMnO₄ tiêu tốn là 29,15 mL. Phản ứng xảy ra như sau:
FeC2O4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + CO2 + K2SO4 + H2O
Giá trị của x là bao nhiêu?
M là muối ngậm nước của sắt có công thức FeC2O4.xH2O. Để xác định x người ta chuẩn độ bằng dung dịch KMnO4 trong môi trường acid H2SO4 loãng và được đun nóng đến 70oC. Lấy 2,6235 gam M hoà tan vào acid H2SO4 loãng và cho thêm nước vào để được 250 mL dung dịch. Lấy 25,00 mL dung dịch này đem chuẩn độ bằng dung dịch KMnO4 0,020 M. Kết quả trung bình của 3 lần chuẩn độ cho thấy thể tích KMnO₄ tiêu tốn là 29,15 mL. Phản ứng xảy ra như sau:
FeC2O4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + CO2 + K2SO4 + H2O
Giá trị của x là bao nhiêu?
Quảng cáo
Trả lời:
5FeC2O4 + 2MnO4− + 16H+→10CO2 + 5Fe3+ + 2Mn2+ + 8H2O
Trong 25,00 mL dung dịch:
Số mol KMnO4 = 0,02. 29,15.10-3 = 5,83.10-4 (mol)
Theo ptpu, số mol của FeC2O4 = 5,83.10-4 = 1,4575.10-3 (mol)
Trong 250 mL dung dịch: số mol của M = số mol của FeC2O4 . 10 = 1,4575.10-2 (mol)
Khối lượng của M = 1,4575.10-2.(56+12.2+16.4+18x) = 2,6235
ð x = 2
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Lời giải
Chọn B
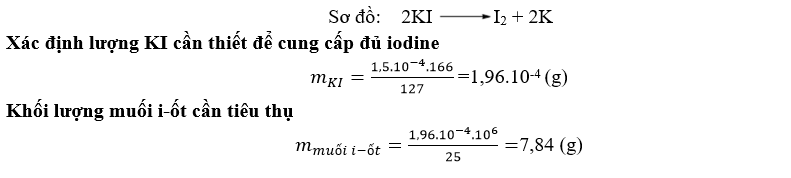
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.






















