Giải thích vì sao tetrachloromethane (CCl4) tuy là phân tử không cực nhưng có nhiệt độ sôi cao hơn trichloromethane (CHCl3) là phân tử có cực
Quảng cáo
Trả lời:
Điều này do phân tử CCl4 có kích thước lớn hơn CHCl3 nên có số electron cũng nhiều hơn CHCl3, do đó tương tác van der Waals giữa các phân tử CCl4 mạnh hơn so với CHCl3 làm cho nhiệt độ sôi của CCl4 cao hơn CHCl3.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
5 nguyên tử H liên kết với C không tham gia vào liên kết hydrogen do độ âm điện của C nhỏ (2,55)
Lời giải
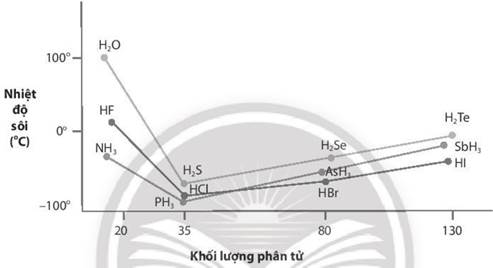
a) Các nguyên tố đầu tiên trong mỗi nhóm VA, VIA, VIIA (N, O, F) có kích thước nhỏ và độ âm điện lớn, nên trong các chất NH3; H2O; HF xuất hiện liên kết hydrogen liên phân tử làm các hợp chất này có nhiệt độ sôi cao bất so với các hợp chất cong lại trong mỗi nhóm.
b) Hợp chất với hydrogen của các nguyên tố còn lại trong mỗi nhóm có nhiệt độ sôi tăng dần khi khối lượng phân tử tăng. Khi khối lượng phân tử tăng làm cho tương tác van der Waals cũng tăng, dẫn đến nhiệt độ sôi tăng lênLời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.