Nhôm (aluminium) được sản xuất bằng phương pháp điện phân Al2O3 tinh khiết. Quặng nhôm thường chứa thạch anh, silicate (chứa Si) và một số tạp chất khác cần được loại bỏ. Một loại quặng bauxite gồm \[A{l_2}{O_3}.3{H_2}O\] và \[10,0{\rm{ }}\% {\rm{ }}kaolin{\rm{ }}A{l_2}S{i_2}{O_7}.2{H_2}O\] được dùng để sản xuất nhôm theo quy trình Bayer. Tính tỉ lệ hao hụt của nhôm trong quá trình tinh chế, biết silic thường được loại bỏ ở dạng bùn aluminosilicate \[\left( {N{a_6}A{l_6}S{i_5}{O_{22}}.5{H_2}O} \right).\] (Làm tròn kết quả đến hàng phần trăm)
Nhôm (aluminium) được sản xuất bằng phương pháp điện phân Al2O3 tinh khiết. Quặng nhôm thường chứa thạch anh, silicate (chứa Si) và một số tạp chất khác cần được loại bỏ. Một loại quặng bauxite gồm \[A{l_2}{O_3}.3{H_2}O\] và \[10,0{\rm{ }}\% {\rm{ }}kaolin{\rm{ }}A{l_2}S{i_2}{O_7}.2{H_2}O\] được dùng để sản xuất nhôm theo quy trình Bayer. Tính tỉ lệ hao hụt của nhôm trong quá trình tinh chế, biết silic thường được loại bỏ ở dạng bùn aluminosilicate \[\left( {N{a_6}A{l_6}S{i_5}{O_{22}}.5{H_2}O} \right).\] (Làm tròn kết quả đến hàng phần trăm)
Câu hỏi trong đề: Đề kiểm tra Hóa 12 Kết nối tri thức Chương 5 có đáp án !!
Quảng cáo
Trả lời:
Hướng dẫn giải
Đáp án đúng là: 7,55.
100 gam quặng chứa 90 gam \(A{l_2}{O_3}.3{H_2}O\)và 10 gam \(A{l_2}S{i_2}{O_7}.2{H_2}O.\)
\[{m_{Al{\rm{ }}max}} = \frac{{2.27.90}}{{156}} + \frac{{2.27.10}}{{258}} = 33,247gam.\]
nAl bị loại bỏ = 1,2nSi = \(\frac{{1,2.2.10}}{{258}} = 0,093\,mol.\)
Tỉ lệ hao hụt nhôm: \(\frac{{0,093.27}}{{33,247}}.100\% = 7,55\% .\)
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Hướng dẫn giải
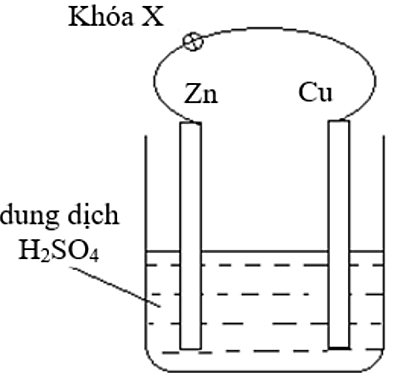
a. Sai. Khi thay thanh Cu bằng thanh Mg, thanh Mg bị ăn mòn điện hóa, do tính khử của Mg mạnh hơn Zn.
b. Đúng. Khi chưa đóng khóa X xảy ra ăn mòn hóa học.
Zn + H2SO4 → ZnSO4 + H2
c. Sai. Tốc độ bọt khí thoát ra khi mở khóa X và khi đóng khóa X là khác nhau. Khi đóng khóa X tốc độ bọt khí diễn ra nhanh hơn.
d. Đúng. Khi đóng khóa X, xảy ra ăn mòn điện hóa và thanh Zn bị ăn mòn.
Lời giải
Hướng dẫn giải
Đáp án đúng là: 3412.
Từ các cặp pin xác định: Tính khử X > Y; T > X; Z > X.
Từ sức điện động chuẩn của pin T - X và Z – X có tính khử: Z > T.
Tính khử: Z > T > X > Y.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.