(1 điểm): Dẫn một lượng dư khí chlorine vào dung dịch chứa hỗn hợp muối NaBr và KBr sau phản ứng thu được hỗn hợp hai muối, đồng thời thấy khối lượng muối giảm 4,45 gam.
Viết các phương trình hoá học xảy ra và tính số mol chlorine đã tham gia phản ứng.
Câu hỏi trong đề: Bộ 3 đề thi cuối kì 2 Hóa 10 Chân trời sáng tạo có đáp án !!
Quảng cáo
Trả lời:
Các phương trình hoá học xảy ra:
Cl2 + 2NaBr → Br2 + 2NaCl
Cl2 + 2KBr → Br2 + 2KCl
Đặt 2 phản ứng trên tương đương với 1 phản ứng là:
Theo bài ra, khối lượng muối giảm 4,45 gam nên:
2x.80 – 2x.35,5 = 4,45 ⇒ x = 0,05 (mol).
Vậy số mol chlorine đã phản ứng là: 0,05 mol.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án đúng là: B
Khi tăng áp suất, các phản ứng (b) và (c) có tốc độ phản ứng thay đổi.
Câu 2
(1) và (2).
(3) và (4).
(1) và (3).
(2) và (4).
Lời giải
Đáp án đúng là: D
> 0, phản ứng thu nhiệt.
Vậy cặp phản ứng thu nhiệt là (2) và (4).
Câu 3
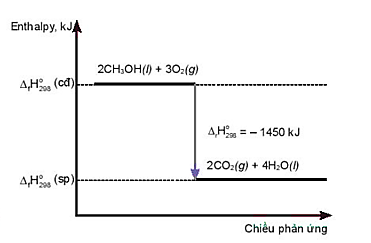
Phản ứng cần cung cấp nhiệt liên tục.
Nhiệt lượng thu vào của phản ứng là – 1450 kJ.
Nhiệt lượng toả ra của phản ứng là 1450 kJ.
Phản ứng thu nhiệt.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
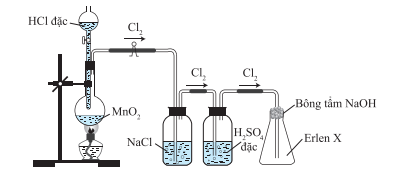
để giữ lại các sản phẩm phụ (HClO, Cl2O…) và không cho chlorine thoát ra ngoài.
để giữ lại hơi nước và không cho chlorine thoát ra ngoài.
để giữ lại khí HCl và không cho oxygen (trong không khí) tác dụng với chlorine.
để giữ lại khí HCl và không cho khí chlorine thoát ra ngoài.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
Phản ứng (1) thu nhiệt, phản ứng (2) toả nhiệt.
Cả hai phản ứng đều toả nhiệt.
Phản ứng (1) toả nhiệt, phản ứng (2) thu nhiệt.
Cả hai phản ứng đều thu nhiệt.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.