Theo QCVN 01-1:2018/BYT, hàm lượng sắt tối đa cho phép trong nước sinh hoạt là 0,30 mg/L. Một mẫu nước có hàm lượng sắt cao gấp 28 lần ngưỡng cho phép, giả thiết sắt trong mẫu nước tồn tại ở dạng Fe2(SO4)3 và FeSO4 với tỉ lệ mol tương ứng là 1 : 8. Quá trình tách loại sắt trong 10 m3 mẫu nước trên được thực hiện bằng cách sử dụng m gam vôi tôi (vừa đủ) để tăng pH, sau đó sục không khí:
Fe2(SO4)3 + Ca(OH)2 → Fe(OH)3 + CaSO4
FeSO4 + Ca(OH)2 + O2 + H2O → Fe(OH)3 + CaSO4
Giả thiết vôi tôi chỉ chứa Ca(OH)2. Giá trị của a là bao nhiêu? (Kết quả làm tròn đến hàng đơn vị)
Quảng cáo
Trả lời:
Đáp án:
122
Đáp án: 122
Fe2(SO4)3 + 3Ca(OH)2 → 2Fe(OH)3 + 3CaSO4
x (mol) 3x
4FeSO4 + 4Ca(OH)2 + O2 + 2H2O → 4Fe(OH)3 + 4CaSO4
8x (mol) 8x
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án:
4
Đáp án: 4
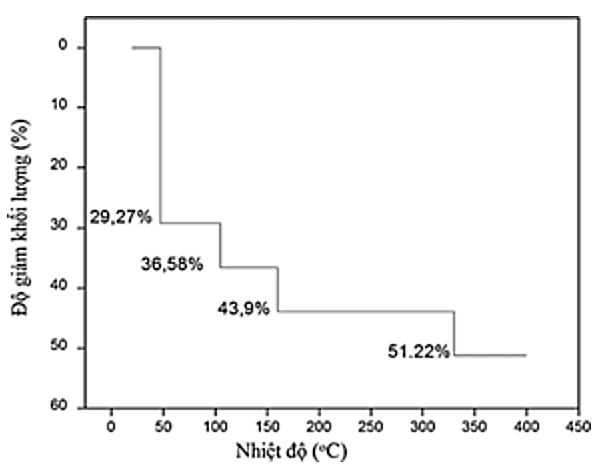
Khi nung nóng đến 400°C, độ giảm khối lượng là 51,22%
Gọi công thức của muối là FeSO4.nH2O
Công thức của muối ở 400°C là MgSO4
Câu 2
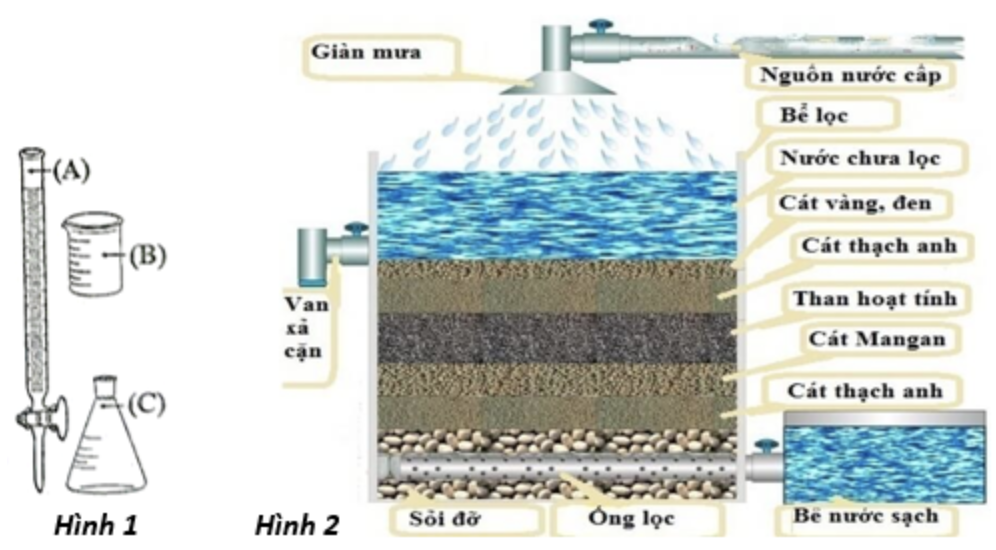
a. Khi chuẩn độ, dung dịch KMnO4 được nhỏ trực tiếp vào bình tam giác từ dụng cụ kí hiệu là (B) được minh họa ở Hình 1.
b. Giá trị của q là 76,6. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười).
c. Giá trị của C2 là 0,003. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần nghìn).
d. Kết quả thu được từ các thí nghiệm phù hợp với giả thuyết ban đầu của nhóm học sinh.
Lời giải
a) Sai
b) Đúng
c) Sai
d) Đúng
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
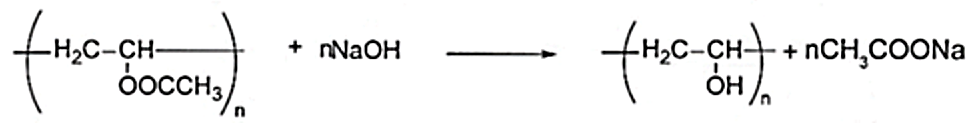
a. Phản ứng trên là phản ứng thủy phân các nhóm chức ester.
b. Phản ứng trên là phản ứng cắt mạch polymer.
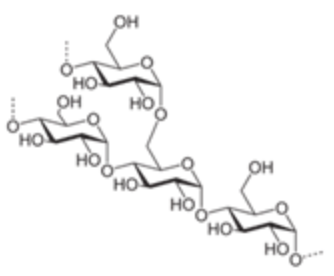
c. Do có nhiều nhóm hydroxy nên PVA có khả năng tan được trong nước.
d. PVA là polyme tổng hợp thân thiện với môi trường.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.