Cellulose là thành phần chính của thành tế bào thực vật, làm nên bộ khung của cây cối. Cellulose có nhiều trong bông, đay, tre, nứa, gỗ,... Từ cellulose người ta điều chế được cellulose acetate (có thành phần chủ yếu là cellulose triacetate và cellulose diacetate) theo các phương trình sau:
[C6H7O2(OH)3]n + 2n(CH3CO)2O → [C6H7O2(OCOCH3)2(OH)]n + 2nCH3COOH
[C6H7O2(OH)3]n + 3n(CH3CO)2O → [C6H7O2(OCOCH3)3]n + 3nCH3COOH
a. Trong mỗi phân tử cellulose có 3 nhóm hydroxy nên cellulose có khả năng phản ứng với Cu(OH)2 trong môi trường kiềm ở nhiệt độ thường tạo dung dịch màu xanh lam.
b. Phân tử khối của cellulose là 162.
c. Bản chất của các phản ứng (1), (2) là nguyên tử H trong nhóm -OH của cellulose được thay bằng nhóm -COCH3.
d. Khi phân tích thành phần nguyên tố của một mẫu cellulose acetate người ta thu được phần trăm khối lượng carbon là 49,875%. Vậy thành phần phần trăm khối lượng oxygen trong cellulose acetate trên là 34,64%. Giả sử trong cellulose acetate chỉ có cellulose triacetate và cellulose diacetate. (kết quả làm tròn đến hàng phần trăm)
Quảng cáo
Trả lời:
a) Sai
b) Sai
c) Đúng
d) Sai
cellulose acetate: [C6H7O2(OCOCH3)x(OH)3-x]n
(2 < x < 3)
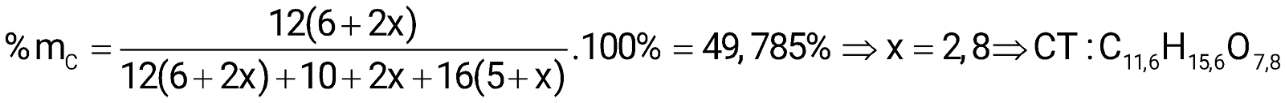
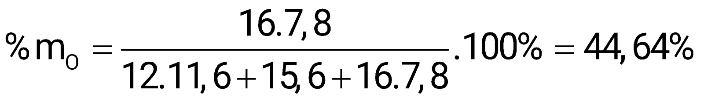
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án:
Đáp án: 77
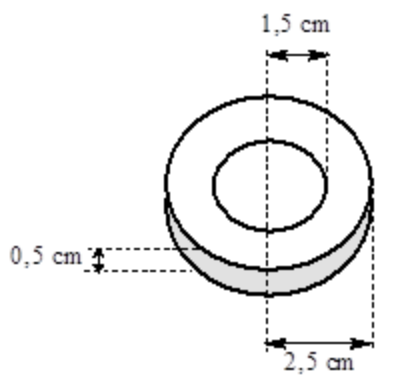
Gọi bán kính vòng ngoài là R, bán kính vòng trong là r, độ dày 0,05 mm = 0,005 cm.
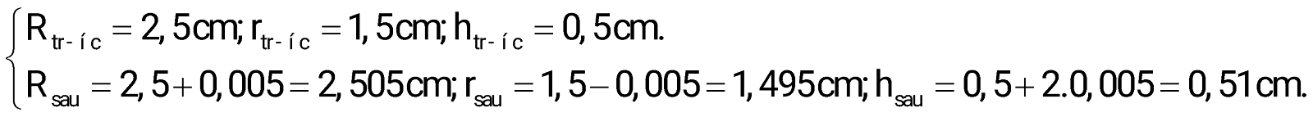
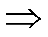
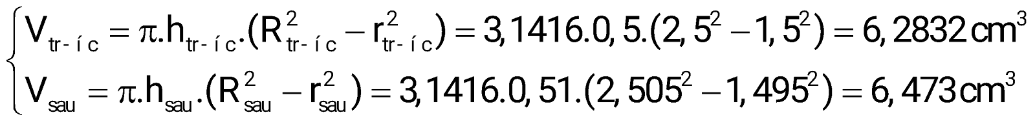
 VNi = 6,473 – 6,2832 = 0,1898 cm3
VNi = 6,473 – 6,2832 = 0,1898 cm3  mNi = 8,9.0,1898 = 1,68922 gam
mNi = 8,9.0,1898 = 1,68922 gam
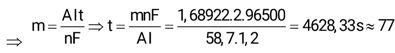
Lời giải
Đáp án:
125
Đáp án: 125
(1) Đúng
(2) Đúng
| Phóng điện | Anode (-): Pb(s) + HSO4-(aq) → PbSO4(s) + H+ (aq) + 2e
Cathode (+): PbO2(s) + HSO4-(aq) + 3H+(aq) + 2e → PbSO4(s) + 2H2O(l) PƯ phóng điện: Pb(s) + PbO2(s) + 2HSO4-(aq) + 2H+(aq) → 2PbSO4(s) + 2H2O(l) |
| Sạc điện | Cathode (-): PbSO4(s) + H+ (aq) + 2e → Pb(s) + HSO4-(aq)
Anode (+): PbSO4(s) + 2H2O(l) → PbO2(s) + HSO4-(aq) + 3H+(aq) + 2e PƯ sạc điện: 2PbSO4(s) + 2H2O(l) → Pb(s) + PbO2(s) + 2HSO4-(aq) + 2H+(aq) |
(3) Sai. q = 60 Ah = 60.3600 = 216000 As hay C
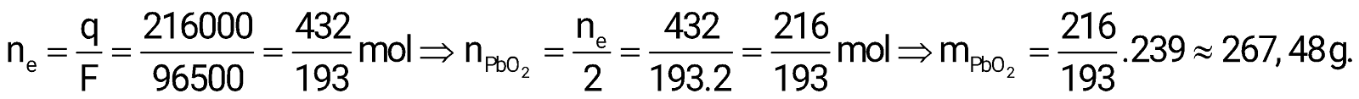
(4) Sai vì PƯ sạc điện: 2PbSO4(s) + 2H2O(l) → Pb(s) + PbO2(s) + 2HSO4-(aq) + 2H+(aq)
(5) Đúng vì khi tỉ trọng của dung dịch bên trong acquy tăng thì lượng H2SO4 tăng (được tạo thành) phù hợp với phản ứng khi acquy sạc điện (HSO4- + H+ chính là H2SO4).
Câu 3
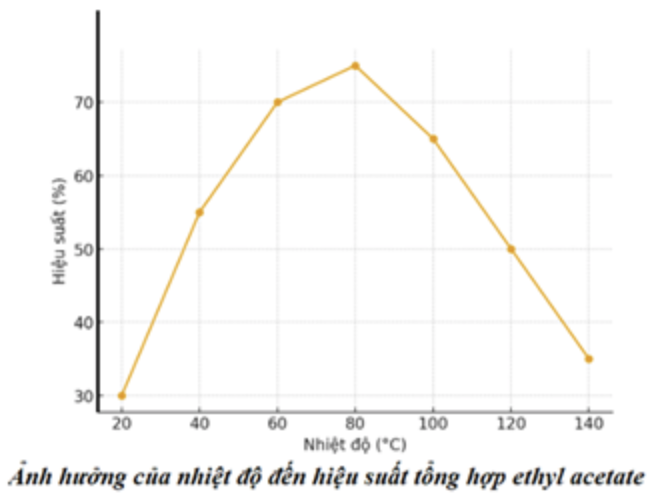
a. Ethyl acetate được tách khỏi hỗn hợp sau phản ứng bằng phương pháp kết tinh.
b. Phản ứng tổng hợp ethyl acetate ở 60°C có hiệu suất thấp hơn ở 120°C.
c. Từ kết quả thí nghiệm có thể kết luận “Khi nhiệt độ càng cao thì hiệu suất phản ứng tổng hợp ethyl acetate càng lớn".
d. Phản ứng tổng hợp ethyl acetate trong thí nghiệm này được gọi là phản ứng ester hoá.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
Ag.
Cu(NO3)2.
AgNO3.
CuSO4.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.