CHẤT CHỈ THỊ ACID – BASE
Thuật ngữ acid hoặc base (acid hoặc kiềm) vẫn thường xuất hiện rất phổ biến trong đời sống gia đình. Để nhận biết một dung dịch có môi trường là acid hay là base người ta sử dụng tới chất chỉ thị acid – base. Chất chỉ thị acid – base là chất có màu sắc biến đổi phụ thuộc vào giá trị pH của dung dịch. Một trong những chất chỉ thị thông dụng nhất trong các kĩ thuật chuẩn độ acid - base đó là phenolphthalein.
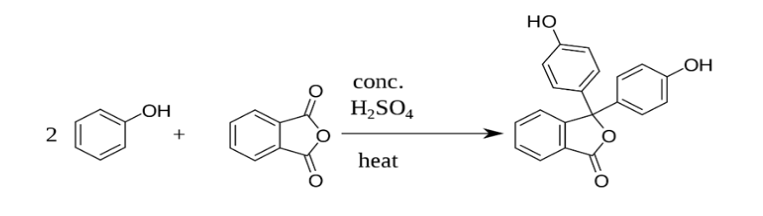
Adolf van Bayer đã phát hiện ra phenolphtalein vào năm 1871. Ông đã quan sát thấy sự hình thành của phenolphtalein khi đun nóng phenol với phthalic anhydride với sự có mặt của acid:
Phenolphthalein là chất rắn kết tinh không màu, đôi khi nó có thể ở dạng bột màu vàng nhạt hoặc màu cam. Đây là một chất không tan trong nước nhưng tan trong cồn. Ở trạng thái tự nhiên, phenolphtalein tồn tại ở dạng acid yếu không màu, được kí hiệu là HIn. Hằng số phân li acid (Ka) của HIn là 3.10− 10 . Base liên hợp của nó có màu đỏ hồng đậm. Trong dung dịch nước, phenolphthalein sẽ có trạng thái cân bằng như sau:
𝐻𝐼𝑛 + 𝐻2𝑂 ⇌ 𝐼𝑛 − + 𝐻3𝑂+
Theo nguyên lý chuyển dịch cân bằng Le Chatelier, trạng thái cân bằng trên sẽ chuyển dịch sang trái nếu nồng độ của H3O+ tăng lên, tức là trong dung dịch ưu tiên chiều phản ứng:
𝐼𝑛− + 𝐻3𝑂+ → 𝐻𝐼𝑛 + 𝐻2𝑂 hơn. Nếu dung dịch có tính base mạnh thì cân bằng chuyển dịch sang phải vì ion OH− sẽ phản ứng với các phân tử HIn chuyển hóa thành In−.
Trong các phép chuẩn độ, phenolphtalein được thêm vào để nhận ra điểm dừng chuẩn độ. Tại điểm này có sự thay đổi màu sắc đột ngột của dung dịch được chuẩn độ vì có sự thay đổi của pH trong môi trường chuẩn độ làm thay đổi trạng thái tồn tại của chất chỉ thị mà, từ đó màu của chỉ thị sẽ thay đổi là một dấu hiệu nhận biết đã đến lúc cần dừng chuẩn độ. Người ta coi rằng có một pH trung gian nào đó một nửa phenolphtalein ở dạng acid và một nửa ở dạng base liên hợp có màu. Độ pH trung gian này có thể được tính theo phương trình Henderson – Hasselbalch cho trạng thái cân bằng chỉ thị: \(pH = pKa + \log \frac{{[I{n^ - }]}}{{[HIn]}}\)
Trả lời cho các câu 75, 76, 77, 78, 79, 80, 81 dưới đây:
Công thức phân tử của hợp chất phenolphtalein là
CHẤT CHỈ THỊ ACID – BASE
Thuật ngữ acid hoặc base (acid hoặc kiềm) vẫn thường xuất hiện rất phổ biến trong đời sống gia đình. Để nhận biết một dung dịch có môi trường là acid hay là base người ta sử dụng tới chất chỉ thị acid – base. Chất chỉ thị acid – base là chất có màu sắc biến đổi phụ thuộc vào giá trị pH của dung dịch. Một trong những chất chỉ thị thông dụng nhất trong các kĩ thuật chuẩn độ acid - base đó là phenolphthalein.
Adolf van Bayer đã phát hiện ra phenolphtalein vào năm 1871. Ông đã quan sát thấy sự hình thành của phenolphtalein khi đun nóng phenol với phthalic anhydride với sự có mặt của acid:

Phenolphthalein là chất rắn kết tinh không màu, đôi khi nó có thể ở dạng bột màu vàng nhạt hoặc màu cam. Đây là một chất không tan trong nước nhưng tan trong cồn. Ở trạng thái tự nhiên, phenolphtalein tồn tại ở dạng acid yếu không màu, được kí hiệu là HIn. Hằng số phân li acid (Ka) của HIn là 3.10− 10 . Base liên hợp của nó có màu đỏ hồng đậm. Trong dung dịch nước, phenolphthalein sẽ có trạng thái cân bằng như sau:
𝐻𝐼𝑛 + 𝐻2𝑂 ⇌ 𝐼𝑛 − + 𝐻3𝑂+
Theo nguyên lý chuyển dịch cân bằng Le Chatelier, trạng thái cân bằng trên sẽ chuyển dịch sang trái nếu nồng độ của H3O+ tăng lên, tức là trong dung dịch ưu tiên chiều phản ứng:
𝐼𝑛− + 𝐻3𝑂+ → 𝐻𝐼𝑛 + 𝐻2𝑂 hơn. Nếu dung dịch có tính base mạnh thì cân bằng chuyển dịch sang phải vì ion OH− sẽ phản ứng với các phân tử HIn chuyển hóa thành In−.
Trong các phép chuẩn độ, phenolphtalein được thêm vào để nhận ra điểm dừng chuẩn độ. Tại điểm này có sự thay đổi màu sắc đột ngột của dung dịch được chuẩn độ vì có sự thay đổi của pH trong môi trường chuẩn độ làm thay đổi trạng thái tồn tại của chất chỉ thị mà, từ đó màu của chỉ thị sẽ thay đổi là một dấu hiệu nhận biết đã đến lúc cần dừng chuẩn độ. Người ta coi rằng có một pH trung gian nào đó một nửa phenolphtalein ở dạng acid và một nửa ở dạng base liên hợp có màu. Độ pH trung gian này có thể được tính theo phương trình Henderson – Hasselbalch cho trạng thái cân bằng chỉ thị: \(pH = pKa + \log \frac{{[I{n^ - }]}}{{[HIn]}}\)
Trả lời cho các câu 75, 76, 77, 78, 79, 80, 81 dưới đây:
Quảng cáo
Trả lời:
Giải chi tiết:
Công thức phân tử của phenolphthalein là C20H14O4.
Đáp án cần chọn là: A
Câu hỏi cùng đoạn
Câu 2:
Chọn các đáp án đúng
Thành phần và cấu trúc của phân tử phenolphthalein gồm
Chọn các đáp án đúng
Thành phần và cấu trúc của phân tử phenolphthalein gồm
Giải chi tiết:
Phenolphtalein gồm:
- Vòng thơm 6 cạnh.
- Phenol
- Ester
- Dị vòng chứa O
Đáp án cần chọn là: A; C; E; F
Câu 3:
Các nhận định dưới đây là đúng hay sai?
Những yếu tố chỉ ra rằng phenolphthalein là acid yếu là:
Các nhận định dưới đây là đúng hay sai?
Những yếu tố chỉ ra rằng phenolphthalein là acid yếu là:
Giải chi tiết:
a đúng. Do có 2 vòng phenol trong cấu trúc nên phenolphthalein thể hiện tính acid yếu.
b sai, nhóm chức của carboxylic acid chỉ thể hiện tính acid, không xác định được độ mạnh - yếu.
c đúng. Hằng số phân li Ka = 3.10-10 là rất nhỏ, chứng tỏ khả năng phân li H+ rất yếu.
Đáp án cần chọn là: Đ; S; Đ
Câu 4:
Điền số thích hợp vào chỗ trống (Làm tròn đến chữ số thập phân thứ nhất)
pH trung gian mà tại đó người ta mong chờ có sự đổi màu của chỉ thị phenolphtalein là ____.
Đáp án đúng là: 9,5
Giải chi tiết:
pH trung gian mà tại đó người ta mong chờ có sự đổi màu của chỉ thị phenolphtalein là
pH = -log( 3.10− 10) = 9,5
Đáp án cần điền là: 9,5
Câu 5:
Cho các từ: không màu, màu hồng, Hin, In-. Điền các từ này vào chỗ trống thích hợp:
Khi cho phenolphthalein vào cốc đựng dung dịch nước chanh có pH = 2,4 thì chỉ thị __________. Khi cho phenolphthalein vào cốc đựng dung dịch Ba(OH)2 nồng độ 0,1M thì nồng độ của ____ trong dung dịch lớn hơn nồng độ của ____
Giải chi tiết:
Khi cho phenolphthalein vào cốc đựng dung dịch nước chanh có pH = 2,4 thì chỉ thị không màu. Khi cho phenolphthalein vào cốc đựng dung dịch Ba(OH)2 nồng độ 0,1M thì nồng độ của In- trong dung dịch lớn hơn nồng độ của HIn.
Đáp án cần chọn là: không màu; In-; HIn
Câu 6:
Để tổng hợp 18 mol phenolphtalein theo quá trình đã được Adolf van Bayer đã phát hiện ra vào năm 1871 cần bao nhiêu gam chất phản ứng? Biết phản ứng có hiệu suất 90%
Giải chi tiết:
\({n_{{\rm{phenol}}}} = 18 \cdot 2:90\% = 40\)mol
\({n_{{\rm{phthalic anhydride}}}} = 18:90\% = 20\)mol
Khi đó m phản ứng\( = 40 \cdot 94 + 20 \cdot 148 = 6720\)gam
Đáp án cần chọn là: D
Câu 7:
Nhận định dưới đây là đúng hay sai?
Nồng độ ion H+ ảnh hưởng tới trạng thái tồn tại của HIn
Nhận định dưới đây là đúng hay sai?
Nồng độ ion H+ ảnh hưởng tới trạng thái tồn tại của HIn
Giải chi tiết:
Nếu nồng độ của H+ tăng lên, cân bằng chuyển dịch sang trái, sẽ tồn tại HIn.
Nếu nồng độ của H+ giảm lên, cân bằng chuyển dịch sang phải, ion OH− sẽ phản ứng với các phân tử HIn chuyển hóa thành In−.
Đáp án cần chọn là: A
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Giải chi tiết:
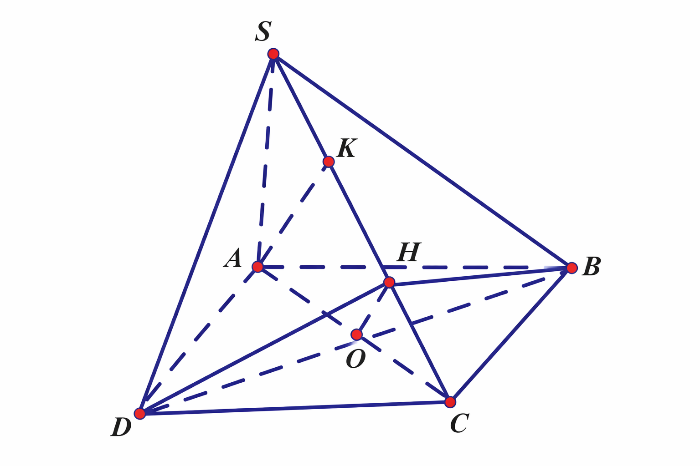
Dựng \(OH \bot SC.\)
Do \(SA \bot (ABCD)\)nên \(SA \bot BD.\)
Mà \(AC \bot BD\)nên \(BD \bot (SAC).\)Suy ra \(BD \bot SC.\)
Mặt khác \(OH \bot SC\)nên \(SC \bot (DHB).\)
Như vậy \(\widehat {DHB}\) là góc giữa hai mặt phẳng \(\left( {SCD} \right)\) và \(\left( {SBC} \right).\)
Tam giác \(ABD\) đều cạnh \(a\) nên \(AO = \frac{{a\sqrt 3 }}{2} \Rightarrow AC = a\sqrt 3 .\)
Dựng \(AK \bot SC \Rightarrow AK = \frac{{SA \cdot OC}}{{\sqrt {S{A^2} + O{C^2}} }} = a \Rightarrow OH = \frac{{AK}}{2} = \frac{a}{2}.\)
Tam giác \(DHB\) có đường trung tuyến \(HO = \frac{1}{2}BD = \frac{a}{2}.\)
\( \Rightarrow \Delta DHB\) vuông tại \(H\) hay Do đó \((SCD) \bot (SBC).\)
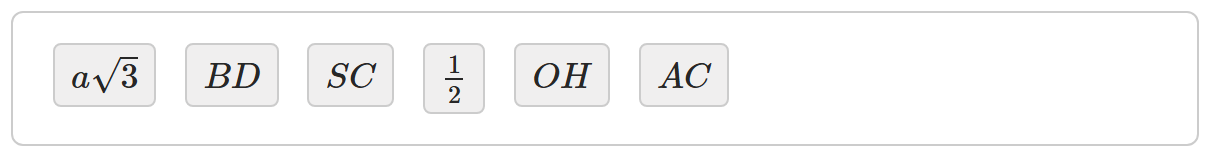
Đáp án cần chọn là: \(BD;AC;SC;OH;\)\(\frac{1}{2}.\)
Câu 2
Lời giải
Giải chi tiết:
Khi chuyển sang môi trường mới, ốc bươu vàng thường không có vật ăn thịt tự nhiên để khống chế số lượng, dẫn đến bùng nổ quần thể và đe dọa cân bằng sinh thái.
Đáp án cần chọn là: C
Câu 3
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.