(1,0 điểm): Tính biến thiên enthalpy chuẩn của phản ứng:
3H2 (g) + N2 (g) → 2NH3 (g)
Biết năng lượng liên kết (kJmol-1) trong các chất như sau:
|
H – H |
N ≡ N |
N – H |
|
436 |
946 |
389 |
Dựa vào kết quả đã tính cho biết phản ứng đã cho tỏa nhiệt hay thu nhiệt.
Câu hỏi trong đề: Bộ 68 đề thi cuối kì 2 Hóa học 10 năm 2023-2024 có đáp án !!
Quảng cáo
Trả lời:
Biến thiên enthalpy chuẩn của phản ứng trên được tính theo năng lượng liên kết là
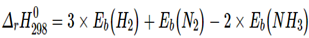
= 3 × Eb (H – H) + Eb (N ≡ N) – 2 × 3 × Eb (N – H)
= 3 × 436 + 946 - 2 × 3 × 389 = -80 kJ. (0,5 điểm)
Kết luận đây là phản ứng tỏa nhiệt (0,5 điểm)
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
những dạng tồn tại bền nhất trong tự nhiên.
những hợp chất bền vững nhất.
những oxide có hóa trị cao nhất.
những đơn chất bền vững nhất.
Lời giải
Đáp án đúng là D
Câu 2
khử.
nhận proton.
oxi hóa
tự oxi hóa – khử.
Lời giải
Đáp án đúng là A
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
(1).
(1) và (3).
(3) và (4).
(2) và (3).
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
92,3 kJ mol-1.
184,6 kJ mol-1.
184,6 kJ mol-1.
92,3 kJ mol-1
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















