Quan sát Hình 16.4 và phương trình hóa học của phản ứng, giải thích vì sao tốc độ mất màu của KMnO4 trong 2 cốc không giống nhau.
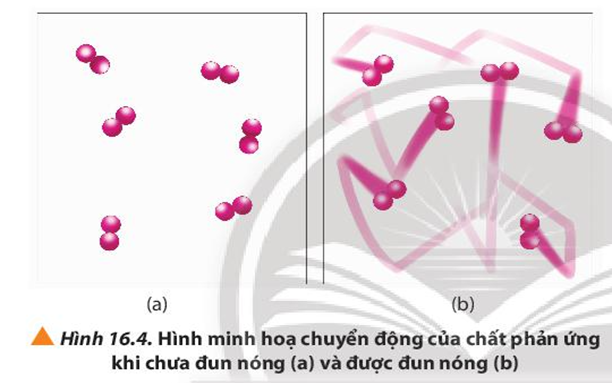
Quan sát Hình 16.4 và phương trình hóa học của phản ứng, giải thích vì sao tốc độ mất màu của KMnO4 trong 2 cốc không giống nhau.

Quảng cáo
Trả lời:
Phương trình hóa học của phản ứng:
2KMnO4(aq) + 5H2C2O4(aq) + 3H2SO4(aq) → 2MnSO4(aq) + K2SO4(aq) + 10CO2(g) + 8H2O(l)
Ở nhiệt độ thường, các chất phản ứng chuyển động với tốc độ nhỏ.
Khi tăng nhiệt độ, các chất sẽ phản ứng sẽ chuyển động với tốc độ lớn hơn, dẫn đến số va chạm hiệu quả tăng nên tốc độ phản ứng tăng.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Khi nhiệt độ tăng thêm 10oC, tốc độ của một phản ứng hóa học tăng 4 lần
⇒ γ = 4
Khi nhiệt độ giảm từ 70oC xuống 40oC thì tốc độ phản ứng giảm 64 lần.
Lời giải
Hệ số nhiệt độ Van’t Hoff γ = 2.
Khi tăng nhiệt độ của phản ứng từ 30oC lên 60oC tốc độ phản ứng tăng 8 lần.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.























