Theo mô hình VSEPR, phân tử formaldehyde có dạng tam giác phẳng. Xác định trạng thái lai hóa của nguyên tử trung tâm carbon. Cho biết formaldehyde có công thức như hình sau đây:
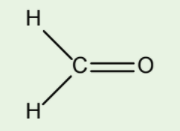
Theo mô hình VSEPR, phân tử formaldehyde có dạng tam giác phẳng. Xác định trạng thái lai hóa của nguyên tử trung tâm carbon. Cho biết formaldehyde có công thức như hình sau đây:

Câu hỏi trong đề: Chuyên đề Hóa 10 Bài 1: Liên kết hóa học có đáp án !!
Quảng cáo
Trả lời:
Cấu hình electron của C (Z = 6) là 1s22s22p2.
1 AO 2s tổ hợp với 2 AO 2p tạo 3 AO lai hóa sp2.
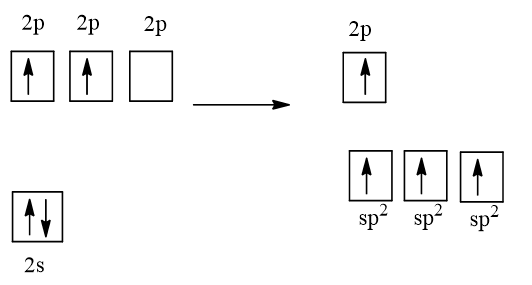
Vậy nguyên tử C trong phân tử formaldehyde lai hóa sp2
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Lưu ý: Có thể dự đoán nhanh trạng thái lai hóa của nguyên tử A (nguyên tố s, p) trong một phân tử bất kì như sau:
- Xác định số nguyên tử liên kết trực tiếp với A.
- Xác định số cặp electron hóa trị riêng của A.
- Nếu tổng hai giá trị là 2; 3 hoặc 4 thì trạng thái lai hóa của A lần lượt là sp; sp2 hoặc sp3
a) Trong phân tử PCl3
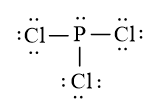
- Số nguyên tử liên kết với P là 3.
- Số cặp electron hóa trị riêng của P là 1
- Tổng hai giá trị là 4 ⇒ Trạng thái lai hóa của C là sp3.
b) Trong phân tử CS2
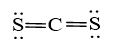
- Số nguyên tử liên kết với C là 2.
- Số cặp electron hóa trị riêng của C là 0
- Tổng hai giá trị là 2 ⇒ Trạng thái lai hóa của C là sp.
c) Trong phân tử SO2
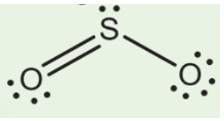
- Số nguyên tử liên kết với S là 2.
- Số cặp electron hóa trị riêng của S là 1
- Tổng hai giá trị là 3 ⇒ Trạng thái lai hóa của S là sp2.
Lời giải
- Từ công thức Lewis của H2O
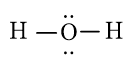
⇒ Công thức VSEPR của H2O là: AX2E2
- Từ công thức Lewis của NH3
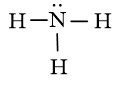
⇒ Công thức VSEPR của NH3 là: AX3E1
- Từ công thức Lewis của SO2
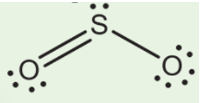
⇒ Công thức VSEPR của SO2 là AX2E1.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















