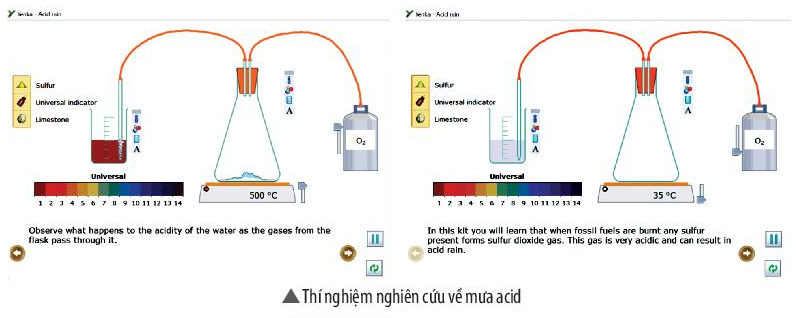
Hãy thiết kế thí nghiệm (thẻ New): Phản ứng của dung dịch iron(II) chloride 1M (FeCl2) với dung dịch potassium hydroxide 1 M (KOH).
a) Ghi rõ các bước chuẩn bị hóa chất, dụng cụ, cách tiến hành thí nghiệm.
b) Nêu hiện tượng xảy ra và giải thích.
Hãy thiết kế thí nghiệm (thẻ New): Phản ứng của dung dịch iron(II) chloride 1M (FeCl2) với dung dịch potassium hydroxide 1 M (KOH).
a) Ghi rõ các bước chuẩn bị hóa chất, dụng cụ, cách tiến hành thí nghiệm.
b) Nêu hiện tượng xảy ra và giải thích.
Quảng cáo
Trả lời:
Bước 1: Nhấp chuột vào thẻ New, chọn Presentation → ![]() rồi kéo ra màn hình làm việc, gõ tên thí nghiệm “Phản ứng của dung dịch iron(II) chloride với dung dịch potassium hydroxide”. Sau đó chọn
rồi kéo ra màn hình làm việc, gõ tên thí nghiệm “Phản ứng của dung dịch iron(II) chloride với dung dịch potassium hydroxide”. Sau đó chọn ![]() (khay để lấy hóa chất, dụng cụ)
(khay để lấy hóa chất, dụng cụ)
Bước 2: Lấy hóa chất
- Chọn Fe: Nhấp chuột vào thẻ Chemicals → Metal → Iron. Kéo thả vào khay.
Nhấp vào thông số khối lượng, điều chỉnh khối lượng Fe về 0,56 gam.
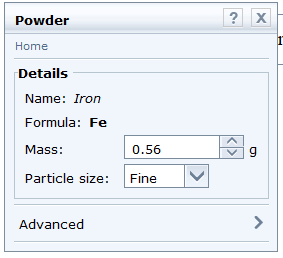
- Chọn hydrochloric acid: Chemicals → Acids → hydrochloric acid. Kéo thả vào khay. Nhấp vào các thông số về nồng độ và thể tích để điều chỉnh cho phù hợp với thí nghiệm. Chọn nồng độ 2 M và thể tích 10 cm3
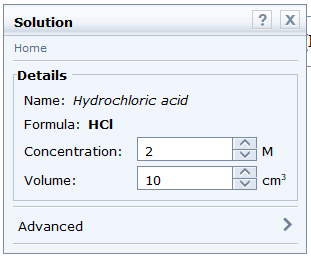
- Chọn dung dịch potassium hydroxide: Chemicals → Alkalis → Potassium hydroxide. Thông số về nồng độ là 1M phù hợp với thí nghiệm nên không cần điều chỉnh.
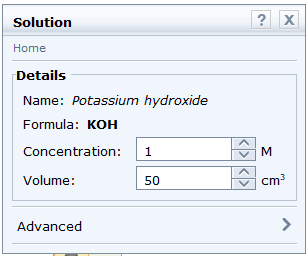
Bước 3: Lấy dụng cụ
- Chọn bình tam giác: Nhấp chuột vào thẻ Glassware → Standard → Erlenmeyer flask
Bước 4: Nhấp nút Play/Pause ![]() trên thanh công cụ. Cho iron (Fe) vào bình tam giác rồi thêm tiếp hydrochloric acid.
trên thanh công cụ. Cho iron (Fe) vào bình tam giác rồi thêm tiếp hydrochloric acid.
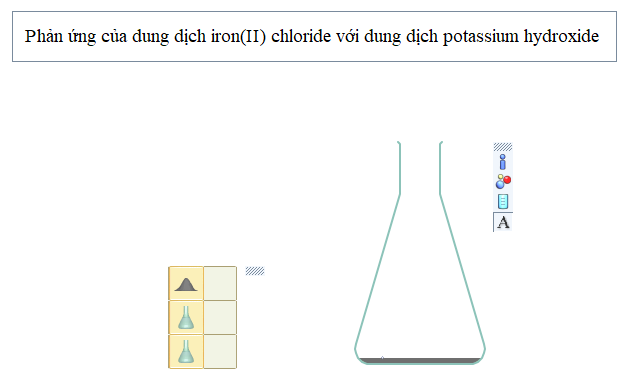
Nhấn nút Play/Pause trên thanh công cụ để thí nghiệm bắt đầu diễn ra, quan sát hiện tượng xảy ra. Muốn phản ứng xảy ra nhanh hay chậm, nhấp chuột vào nút Simulation Speed ![]()
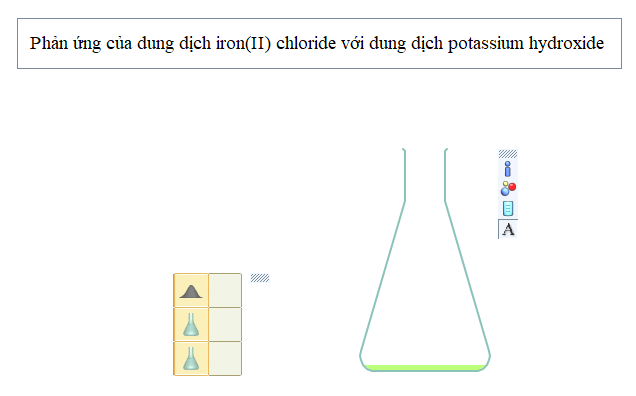
Nhấp nút Play/Pause ![]() trên thanh công cụ. Cho tiếp dung dịch potassium hydroxide vào bình tam giác:
trên thanh công cụ. Cho tiếp dung dịch potassium hydroxide vào bình tam giác:
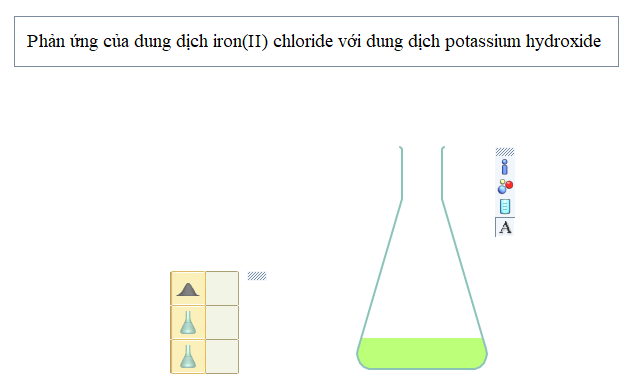
Nhấn nút Play/Pause trên thanh công cụ để thí nghiệm bắt đầu diễn ra, quan sát hiện tượng xảy ra. Muốn phản ứng xảy ra nhanh hay chậm, nhấp chuột vào nút Simulation Speed ![]()
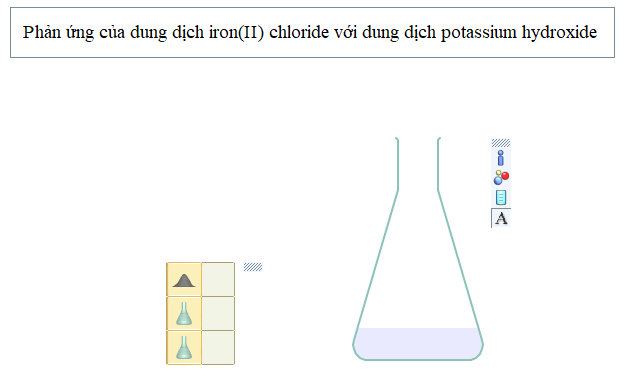
Bước 5: Sau khi các chất phản ứng với nhau, nhấn chuột vào các icon bên phải của dụng cụ để biết các thông tin:
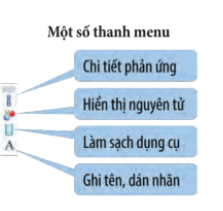
Bước 6: Quan sát – Giải thích thí nghiệm
Hiện tượng:
- Đầu tiên iron (Fe) tan trong HCl để được dung dịch màu xanh, có khí thoát ra (coi thể tích dung dịch thay đổi không đáng kể sau phản ứng);
- Thêm tiếp dung dịch potassium hydroxide vào bình phản ứng thu được kết tủa màu trắng hơi xanh;
Giải thích bằng phương trình hóa học:
Fe + 2HCl → FeCl2 + H2↑
FeCl2 + 2KOH → Fe(OH)2↓ + 2KCl
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Bước 1: Bấm vào hình tam giác sẽ xuất hiện bảng mức độ thể hiện khác nhau.
Các dụng dịch có sẵn (Introduction) và tự tạo dung dịch (My Solution). Chọn Introduction
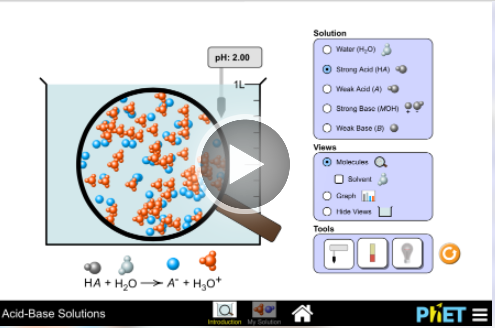

Bước 2: Sau đó hiện màn hình hiển thị thí nghiệm.
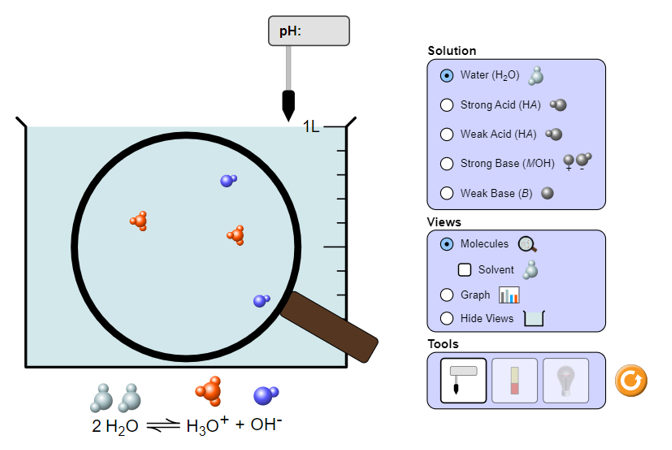
- Chọn các dung dịch cần đo pH ở mục Solution.
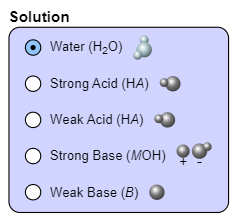
- Chọn chế độ quan sát:
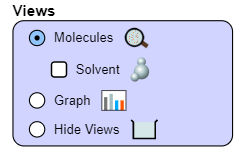
+ Dạng phân tử (Molecules)
+ Hiện cả phân tử dung môi nhấn chọn Solvent.
+ Dạng đồ thị biểu diễn nồng độ chất tan trong dung dịch (Graph)
+ Ẩn chế độ xem (Hide Views)
- Các công cụ (dụng cụ):
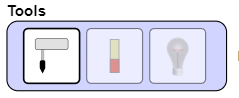
+ Đo pH bằng máy đo.
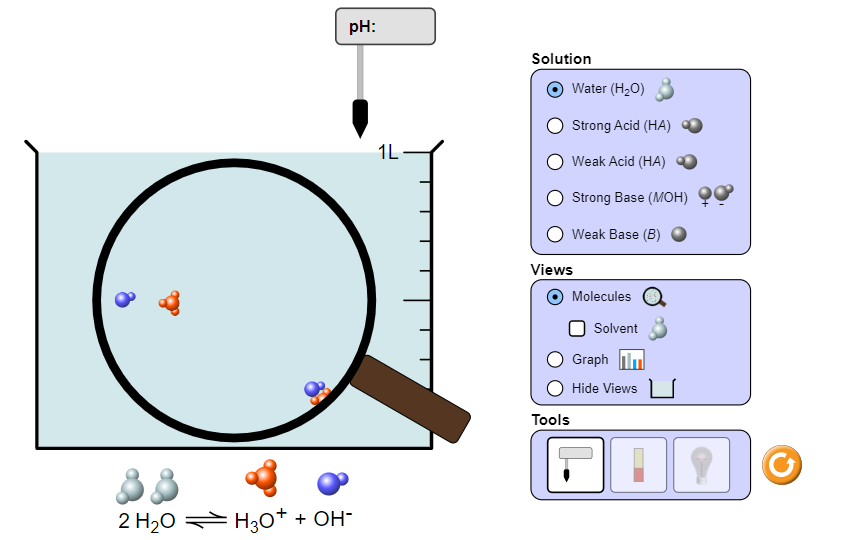
+ Đo pH bằng giấy chỉ thị
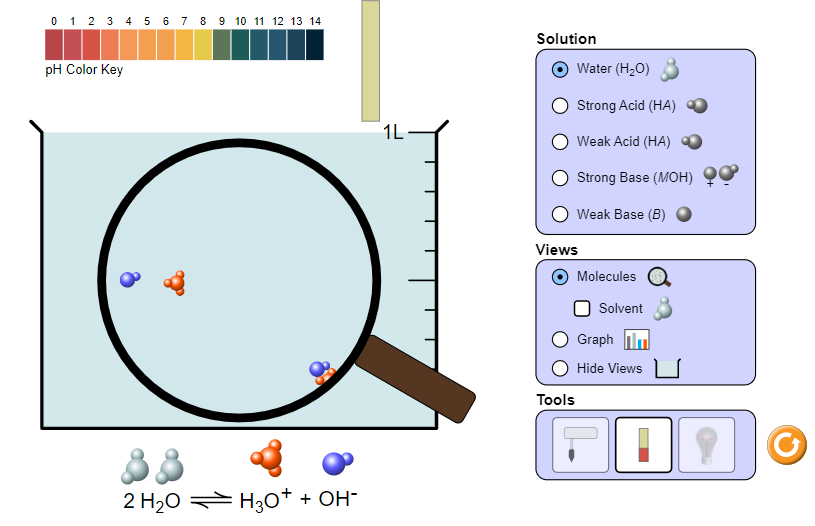
+ Đo độ dẫn điện của dung dịch
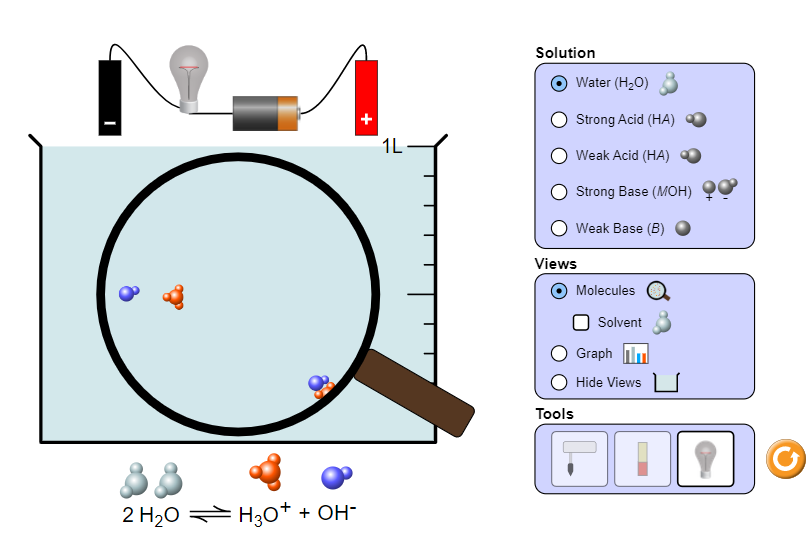
Bước 3: Thực hiện quan sát và ghi lại các kết quả
- Hiển thị các dung dịch dưới dạng phân tử hoặc đồ thị.
Ví dụ:
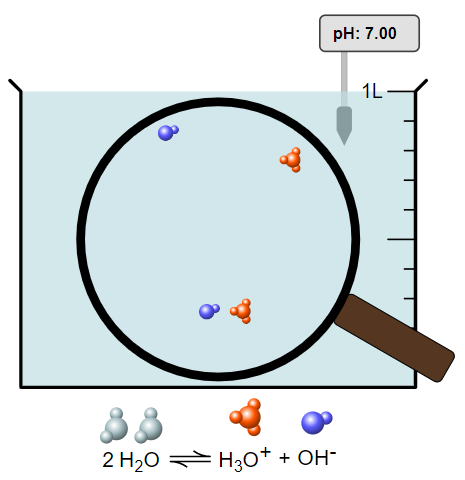
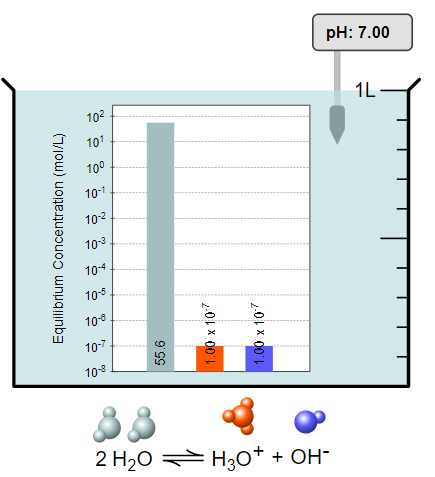
- Thực hiện thí nghiệm với các dụng cụ (công cụ) khác nhau được cung cấp trong mô phỏng.
Ví dụ:
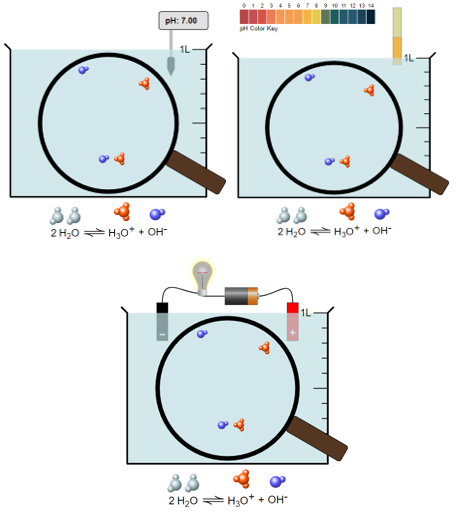
- Nhận xét về giá trị pH của dung dịch acid – base.
|
Dung dịch |
Giá trị pH |
|
Water (H2O) |
7 |
|
Strong Acid (HA) (acid mạnh) |
2 |
|
Weak Acid (HA) (acid yếu) |
4.5 |
|
Strong Base (MOH) (base mạnh) |
12 |
|
Weak Base (B) (base yếu) |
9.5 |
pH chỉ thị mức độ acid hoặc base của một dung dịch. Trong môi trường nước (môi trường trung tính) pH bằng 7. Dưới giá trị này dung dịch có tính acid, trên giá trị này dung dịch có tính base.
Giá trị pH càng lớn tính acid càng giảm và tính base càng tăng.
Lời giải
Bước 1: Nhấp chuột vào thẻ New, chọn Presentation → ![]() rồi kéo ra màn hình làm việc, gõ tên thí nghiệm “Điều chế khí sulfur dioxide từ sulfur và oxygen”. Sau đó chọn
rồi kéo ra màn hình làm việc, gõ tên thí nghiệm “Điều chế khí sulfur dioxide từ sulfur và oxygen”. Sau đó chọn ![]() (khay để lấy hóa chất, dụng cụ)
(khay để lấy hóa chất, dụng cụ)
Bước 2: Lấy hóa chất
- Chọn sulfur: Nhấp chuột vào thẻ Chemicals → Metals → Miscellaneous → Powders → Sulfur, rồi kéo vào vùng làm thí nghiệm. Nếu thí nghiệm nhiều hóa chất và dụng cụ nên cho vào khay.
- Chọn oxygen: Nhấp chuột vào thẻ Chemicals → Metals → Gases → Oxygen, thả sang màn hình hoặc vào khay.
Bước 3: Lấy dụng cụ
- Chọn bình tam giác: Nhấp chuột vào thẻ Glassware → Standard → Erlenmayer flask
- Chọn nút cao su có cắm ống thủy tinh: Nhấp chuột vào thẻ Equipment → Stoppers → Large → One tube
- Chọn bếp điện: Nhấp chuột vào thẻ Equipment → Apparatus → Electric heater
Sắp xếp các dụng cụ như sau:
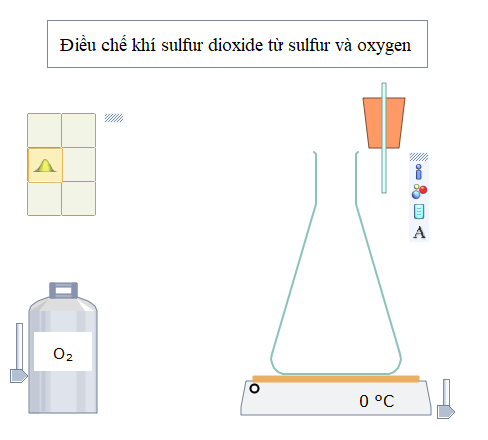
Bước 4: Nhấp nút Play/Pause ![]() trên thanh công cụ. Thêm sulfur vào bình tam giác, đậy nắp, nối với bình oxygen, chỉnh nhiệt độ trên bếp điện như hình bên dưới:
trên thanh công cụ. Thêm sulfur vào bình tam giác, đậy nắp, nối với bình oxygen, chỉnh nhiệt độ trên bếp điện như hình bên dưới:
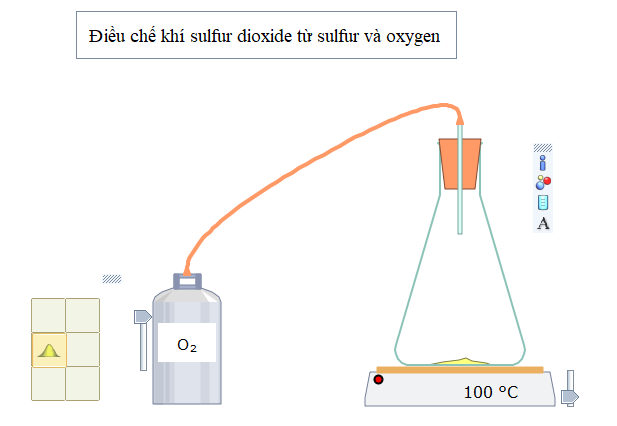
Bước 5: Nhấn nút Play/Pause trên thanh công cụ để thí nghiệm bắt đầu diễn ra, quan sát hiện tượng xảy ra. Muốn phản ứng xảy ra nhanh hay chậm, nhấp chuột vào nút Simulation Speed ![]()
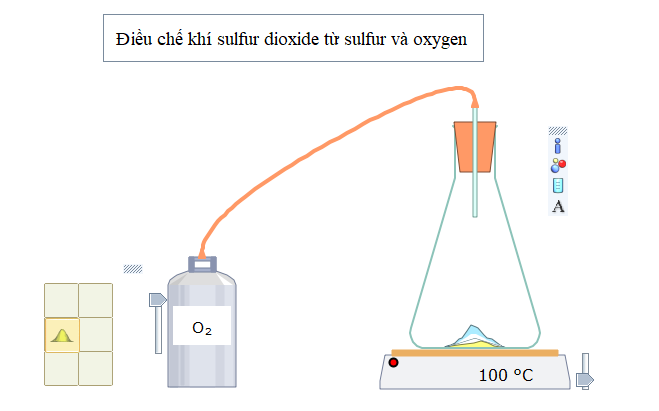
Sau khi các chất phản ứng với nhau, nhấn chuột vào các icon bên phải của dụng cụ để biết các thông tin:
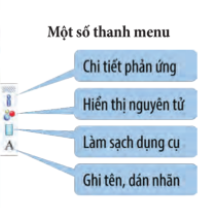
Bước 6: Quan sát – Giải thích thí nghiệm
Hiện tượng:
Sulfur cháy trong oxygen với ngọn lửa màu xanh;
Kết thúc phản ứng thu được khí không có màu;
Phương trình hóa học:
S + O2 SO2
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.