Dựa vào Bảng 18.4, hãy cho biết quá trình phân huỷ 1 mol muối carbonate của nguyên tố nhóm IIA nào cần hấp thu nhiều năng lượng hơn.
Dựa vào Bảng 18.4, hãy cho biết quá trình phân huỷ 1 mol muối carbonate của nguyên tố nhóm IIA nào cần hấp thu nhiều năng lượng hơn.
Quảng cáo
Trả lời:
Dựa vào Bảng 18.4: Giá trị biến thiên enthalpy chuẩn của phản ứng phân huỷ muối carbonate của một số nguyên tố nhóm IIA và xu hướng biến đổi nhiệt độ phân huỷ
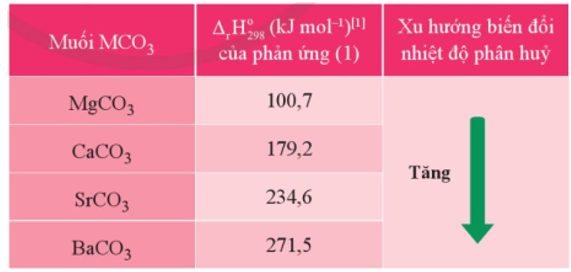
Ta thấy, quá trình phân huỷ 1 mol muối carbonate của nguyên tố barium cần nhiều năng lượng nhất do biến thiên enthalpy chuẩn của phản ứng phân huỷ BaCO3 lớn nhất.
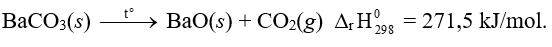
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Hiện tượng:
- Ống nghiệm (1) xuất hiện kết tủa trắng. Ống nghiệm (2) xuất hiện vẩn đục trắng.
- Thời điểm xuất hiện kết tủa ở ống nghiệm (1): ngay sau khi cho dung dịch CuSO4 vào. Thời điểm xuất hiện kết tủa ở ống nghiệm (2): sau khi cho dung dịch CuSO4 vào một lúc.
Phương trình hóa học:
BaCl2(aq) + CuSO4(aq) ⟶ CuCl2(aq) + BaSO4(s)
CaCl2(aq) + CuSO4(aq) ⟶ CuCl2(aq) + CaSO4(s)
Giải thích: Vì BaSO4 không tan trong nước còn CaSO4 ít tan trong nước.
Lời giải
Các rạn san hô và núi đá vôi có thành phần chính là CaCO3.
Mà CaCO3 phản ứng được với nước có carbon dioxide hòa tan theo phương trình hóa học:
CaCO3(s) + H2O(l) + CO2(aq) ⇌ Ca(HCO3)2(aq)
Khi tăng nồng độ của carbon dioxide trong nước biển thì cân bằng hóa học trên sẽ chuyển dịch theo chiều làm giảm nồng độ của carbon dioxide, tức là chiều của phản ứng thuận. Nên lượng CaCO3(s) bị giảm đi.
Do đó, khi có sự gia tăng nồng độ của carbon dioxide trong nước biển thì các rạn san hô và núi đá vôi có thể bị phá huỷ, xói mòn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















