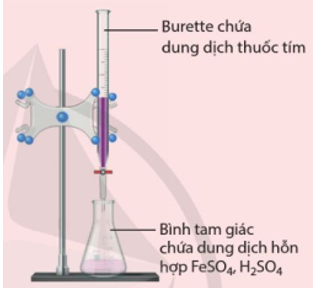
Thí nghiệm 2. Kiểm tra sự có mặt của cation Cu2+ hoặc Fe3+ trong dung dịch
Chuẩn bị:
- Hoá chất: Các dung dịch CuSO4 0,1 M; FeCl3 0,1 M; NaOH 0,1 M.
- Dụng cụ: Ống nghiệm, ống hút nhỏ giọt.
Tiến hành:
- Cho khoảng 4 – 6 giọt dung dịch NaOH vào ống nghiệm chứa khoảng 1 mL dung dịch CuSO4.
- Cho khoảng 4 – 6 giọt dung dịch NaOH vào ống nghiệm chứa khoảng 1 mL dung dịch FeCl3.
Yêu cầu: Quan sát, giải thích hiện tượng và viết phương trình hoá học minh hoạ.
Thí nghiệm 2. Kiểm tra sự có mặt của cation Cu2+ hoặc Fe3+ trong dung dịch
Chuẩn bị:
- Hoá chất: Các dung dịch CuSO4 0,1 M; FeCl3 0,1 M; NaOH 0,1 M.
- Dụng cụ: Ống nghiệm, ống hút nhỏ giọt.
Tiến hành:
- Cho khoảng 4 – 6 giọt dung dịch NaOH vào ống nghiệm chứa khoảng 1 mL dung dịch CuSO4.
- Cho khoảng 4 – 6 giọt dung dịch NaOH vào ống nghiệm chứa khoảng 1 mL dung dịch FeCl3.
Yêu cầu: Quan sát, giải thích hiện tượng và viết phương trình hoá học minh hoạ.
Quảng cáo
Trả lời:
Hiện tượng:
- Ở ống nghiệm chứa dung dịch CuSO4: xuất hiện kết tủa màu xanh, đó là Cu(OH)2.
- Ở ống nghiệm chứa dung dịch FeCl3: xuất hiện kết tủa màu nâu đỏ, đó là Fe(OH)3.
Phương trình hóa học:
2NaOH(aq) + CuSO4(aq) ⟶ Cu(OH)2(s) + Na2SO4(aq)
3NaOH(aq) + FeCl3(aq) ⟶ Fe(OH)3(s) + 3NaCl(aq)
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Số oxi hóa của Fe trong FeO là +2.
Số oxi hóa của Fe trong Fe2O3 là +3.
Số oxi hóa của Fe trong Fe3O4 là +8/3 (hay +2 và + 3).
Lời giải
Phương trình hóa học:
5Fe2+(aq) + (aq) + 8H+(aq) →5Fe3+(aq) + Mn2+(aq) + 4H₂O(1)
Ta có:
Theo phương trình: ![]() = 5 . 1,08 . 10-4 = 5,4 . 10-4 (mol)
= 5 . 1,08 . 10-4 = 5,4 . 10-4 (mol)
a) Khối lượng sắt có trong mẫu chất là: 56 . 5,4 . 10-4 = 0,03024 (g) = 30,24 (mg)
b) Ta có: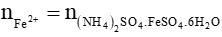 = 5,4 . 10-4 (mol)
= 5,4 . 10-4 (mol)
⇒
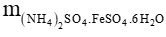 = 392 . 5,4 . 10-4 = 0,21168 (g)
= 392 . 5,4 . 10-4 = 0,21168 (g)
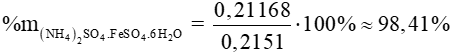
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.