Sử dụng bảng giá trị enthalpy tạo thành chuẩn của một số chất sau cho Câu 11, 12.
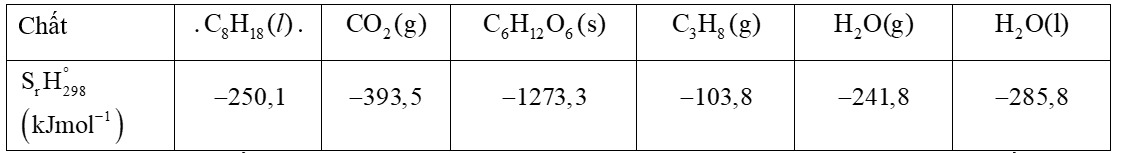
Một thành phố 100 000 dân sử dụng khoảng 1,0 . 1011 kJ năng lượng mỗi ngày. Giả sử, tất cả năng lượng đó đến từ quá trình đốt cháy octane lỏng (C8H18) để tạo thành nước ở thể khí và khí carbon dioxide.
a) Sử dụng enthalpy tạo thành chuẩn để tính biến thiên enthalpy chuẩn cho quá trình đốt cháy octane.
b) Xác định số kg octane cần thiết để cung cấp năng lượng cho thành phố mỗi ngày.
c) Xác định lượng CO2 (mol) phát thải khi tiêu thụ số kg octane nói trên.
d) Nếu thay octane bằng một nhiên liệu khác, ví dụ propane C3H8(g) thì nhiên liệu nào (octane hay propane) sẽ ít ảnh hưởng tới sự nóng lên của toàn cầu hơn?
Sử dụng bảng giá trị enthalpy tạo thành chuẩn của một số chất sau cho Câu 11, 12.

Một thành phố 100 000 dân sử dụng khoảng 1,0 . 1011 kJ năng lượng mỗi ngày. Giả sử, tất cả năng lượng đó đến từ quá trình đốt cháy octane lỏng (C8H18) để tạo thành nước ở thể khí và khí carbon dioxide.
a) Sử dụng enthalpy tạo thành chuẩn để tính biến thiên enthalpy chuẩn cho quá trình đốt cháy octane.
b) Xác định số kg octane cần thiết để cung cấp năng lượng cho thành phố mỗi ngày.
c) Xác định lượng CO2 (mol) phát thải khi tiêu thụ số kg octane nói trên.
d) Nếu thay octane bằng một nhiên liệu khác, ví dụ propane C3H8(g) thì nhiên liệu nào (octane hay propane) sẽ ít ảnh hưởng tới sự nóng lên của toàn cầu hơn?
Quảng cáo
Trả lời:
a) \( - 5074,1\;{\rm{kJ}}\); b) \(2,{3.10^6}\;{\rm{kg}}\); c) \(1,{58.10^8}\;{\rm{mol}}\); d) propane.
\({{\rm{C}}_8}{{\rm{H}}_{18}}(l) + \frac{{25}}{2}{{\rm{O}}_2}(g) \to 8{\rm{C}}{{\rm{O}}_2}(g) + 9{{\rm{H}}_2}{\rm{O}}(g)\)
a) .
b) Số kg octane cần là:
\(\frac{{ - 1,0 \cdot {{10}^{11}}}}{{ - 5074,1 \cdot 114}} = 2,3 \cdot {10^9}(\;{\rm{g}}) = 2,3 \cdot {10^6}(\;{\rm{kg}}){\rm{. }}\)
c) Số mol CO 2 phát thải là: \(\frac{{ - 1,0 \cdot {{10}^{11}}}}{{ - 5074,1 \cdot 8}} = 1,58 \cdot {10^8}(\;{\rm{mol}})\).
d) \({{\rm{C}}_3}{{\rm{H}}_8}(g) + 5{{\rm{O}}_2}(g) \to 3{\rm{C}}{{\rm{O}}_2}(g) + 4{{\rm{H}}_2}{\rm{O}}(g)\)
Số mol CO2 phát thải là: \(\frac{{ - 1,0 \cdot {{10}^{11}}}}{{ - 2043,9 \cdot 3}} = 1,47 \cdot {10^8}(\;{\rm{mol}})\).
Câu hỏi cùng đoạn
Câu 2:
Trong quá trình quang hợp, thực vật sử dụng năng lượng từ ánh sáng mặt trời để tạo thành glucose (C6H12O6) và oxygen từ khí CO2 và H2O(l). Viết phương trình cân bằng cho quá trình quang hợp của cây xanh và tính xem để tạo thành 1 mol glucose, cây xanh cần cung cấp một năng lượng là bao nhiêu kJ?
Trong quá trình quang hợp, thực vật sử dụng năng lượng từ ánh sáng mặt trời để tạo thành glucose (C6H12O6) và oxygen từ khí CO2 và H2O(l). Viết phương trình cân bằng cho quá trình quang hợp của cây xanh và tính xem để tạo thành 1 mol glucose, cây xanh cần cung cấp một năng lượng là bao nhiêu kJ?
Đáp án:
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
A. 430,5 kJ mol-1.
Lời giải
Chọn đáp án A
\({E_b}({\rm{H}} - {\rm{Cl}}) = \left( {\frac{1}{2} \cdot 243 + \frac{1}{2} \cdot 436} \right) - ( - 91) = 430,5\left( {\;{\rm{kJ}}\;{\rm{mo}}{{\rm{l}}^{ - 1}}} \right)\)
Câu 2
A. \({\rm{Al}}(s) + 3{\rm{C}}{{\rm{l}}_2}(g) \to {\rm{AlC}}{{\rm{l}}_3}(s).\)
B. \({\rm{Al}}(s) + 3{\rm{Cl}}(g) \to {\rm{AlC}}{{\rm{l}}_3}(s).\)
C. \(3{\rm{HCl}}(aq) + {\rm{Al}}{({\rm{OH}})_3}(s) \to {\rm{AlC}}{{\rm{l}}_3}(s) + 3{{\rm{H}}_2}{\rm{O}}(l).\)
Lời giải
Chọn đáp án D
Câu 3
A. \({{\rm{O}}_3},{\rm{C}}{{\rm{O}}_2},{\rm{N}}{{\rm{H}}_3},{\rm{HI}}.\)
B. \({\rm{C}}{{\rm{O}}_2},{\rm{N}}{{\rm{H}}_3},{\rm{HI}},{{\rm{O}}_3}.\)
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
A. Cả phản ứng và môi trường xung quanh đều mất một năng lượng là 65 kJ.
B. Cả phản ứng và môi trường xung quanh đều thu được một năng lượng 65 kJ.
C. Phản ứng mất 65 kJ năng lượng và môi trường xung quanh nhận được một năng lượng 65 kJ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
A. 130 kJ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















