12 Bài tập Tính biến thiên enthalpy của phản ứng theo năng lượng liên kết (có lời giải)
36 người thi tuần này 4.6 484 lượt thi 12 câu hỏi 45 phút
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Bài tập Thành phần của nguyên tử lớp 10 (có lời giải)
Bài tập Muối carbnate tác dụng với Hydrochloride acid lớp 10 (có lời giải)
Bài tập Basic oxide tác dụng với Hydrochloride acid lớp 10 (có lời giải)
Bài tập Kim loại tác dụng với Hydrochloride acid lớp 10 (có lời giải)
Bài tập Tính hệ số nhiệt độ Van't Hoff lớp 10 (có lời giải)
Bài tập Tính tốc độ tức thời của phản ứng lớp 10 (có lời giải)
Danh sách câu hỏi:
Câu 1/12
A. -113 kJ.
B. +113 kJ.
C. -527 kJ.
D. +527 kJ.
Lời giải
Đáp án đúng là: A
Biến thiên enthalpy chuẩn của phản ứng trên được tính theo năng lượng liên kết là
\[{\Delta _r}H_{298}^0 = 1 \times {E_b}(C{H_4}) + 1 \times {E_b}(C{l_2}) - 1 \times {E_b}(C{H_3}Cl) - 1 \times {E_b}(HCl)\]
= 1 × 4EC – H + 1 × ECl – Cl – 1 × (3EC – H + EC – Cl) – 1 × EH – Cl
= 1 × 4 × 414 + 1 × 243 - 1×(3×414 + 339) - 1×431 = -113 (kJ).
Câu 2/12
A. +105 kJ.
B. -105 kJ.
C. +986 kJ.
D. -986 kJ.
Lời giải
Đáp án đúng là: B
Biến thiên enthalpy chuẩn của phản ứng trên được tính theo năng lượng liên kết là
\[{\Delta _r}H_{298}^0 = 3 \times {E_b}({H_2}) + {E_b}({N_2}) - 2 \times {E_b}(N{H_3})\]
= 3 × Eb (H – H) + Eb (N ≡ N) – 2 × 3 × Eb (N – H)
= 3 × 432 + 945 - 2 × 3 × 391 = -105 kJ.
Câu 3/12
A. +158 kJ.
B. -158 kJ.
C. +185 kJ.
D. -185 kJ.
Lời giải
Đáp án đúng là: D
Biến thiên enthalpy chuẩn của phản ứng là:
\[\begin{array}{l}{\Delta _r}H_{298}^0 = {E_b}_{(H - H)} + {E_{b(Cl - Cl)}} - 2{E_{b(H - Cl)}}\\ = 436 + 243 - 2.432 = - 185(kJ).\end{array}\]
Câu 4/12
A. -560 kJ.
B. -506 kJ.
C. +560 kJ.
D. +506 kJ.
Lời giải
Đáp án đúng là: B
Biến thiên enthalpy chuẩn của phản ứng là
\({\Delta _r}H_{298}^o = {\rm{ }}2.{E_b}\left( {{H_2}} \right){\rm{ }} + {\rm{ }}{E_b}\left( {{O_2}} \right){\rm{ }}--{\rm{ }}2.{E_b}\left( {{H_2}O} \right)\)
= 2.Eb(H-H) + Eb(O=O) – 2.2.Eb(O-H) = 2.432 + 498 – 2.2.467 = -506 (kJ).
Câu 5/12
A. -3734 kJ.
B. +3734 kJ.
C. -46 kJ.
D. +46 kJ.
Lời giải
Đáp án đúng là: A
Biến thiên enthalpy chuẩn của phản ứng là
\({\Delta _r}H_{298}^o = {\rm{ }}{E_b}\left( {{C_7}{H_{16}}} \right){\rm{ }} + {\rm{ }}11.{E_b}\left( {{O_2}} \right){\rm{ }}--{\rm{ }}7.{E_b}\left( {C{O_2}} \right){\rm{ }}--{\rm{ }}8.{E_b}\left( {{H_2}O} \right)\)
= 6.Eb(C-C) + 16Eb(C-H) + 11.Eb(O=O) – 7.2.Eb(C=O) – 8.2.Eb(O-H)
= 6.347 + 16.413 + 11.498 – 7.2.745 – 8.2.467 = -3734 kJ.
Lời giải
Đáp án đúng là: C
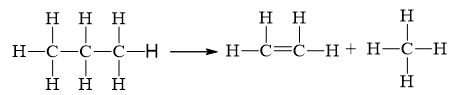
\({\Delta _r}H_{298}^o = 2.{E_b}_{\left( {C{\rm{ }}--{\rm{ }}C} \right)}{\rm{ }} + {\rm{ }}8.{E_b}_{\left( {C{\rm{ }}--{\rm{ }}H} \right)} - 1.{E_b}_{\left( {C{\rm{ }} = {\rm{ }}C} \right)}{\rm{ - }}8.{E_b}_{\left( {C{\rm{ }}--{\rm{ }}H} \right)}\)
= 2.346 + 8.418 - 1.612 - 8.418 = +80 kJ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 8/12
A. -169 kJ.
B. +169 kJ.
C. -196 kJ.
D. +196 kJ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 9/12
A. 305.
B. 360.
C. 464.
D. 837.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 10/12
A. \[{\Delta _r}H_{298K}^o = m \times {\Delta _f}H_{298}^o\left( M \right) + n \times {\Delta _f}H_{298}^o\left( N \right) + a \times {\Delta _f}H_{298}^o\left( A \right) + b \times {\Delta _f}H_{298}^o\left( B \right)\]
B. \[{\Delta _r}H_{298K}^o = a \times {\Delta _f}H_{298}^o\left( A \right) + b \times {\Delta _f}H_{298}^o\left( B \right) - m \times {\Delta _f}H_{298}^o\left( M \right) - n \times {\Delta _f}H_{298}^o\left( N \right)\]
C. \[{\Delta _r}H_{298K}^o = a \times {E_b}\left( A \right) + b \times {E_b}\left( B \right) - m \times {E_b}\left( M \right) - n \times {E_b}\left( N \right)\]
D. \[{\Delta _r}H_{298K}^o = m \times {E_b}\left( M \right) + n \times {E_b}\left( N \right) - a \times {E_b}\left( A \right) - b \times {E_b}\left( B \right)\]
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 11/12
A. +105 kJ.
B. -105 kJ.
C. +150 kJ.
D. -150 kJ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 12/12
A. \[{\Delta _r}H_{298}^0 = {\Delta _f}H_{298}^0\left( {{C_2}{H_5}OH} \right){\rm{ + }}{\Delta _f}H_{298}^0\left( {{C_2}{H_4}} \right){\rm{ + }}{\Delta _f}H_{298}^0\left( {{H_2}O} \right)\]
B. \[{\Delta _f}H_{298}^0 = {\Delta _r}H_{298}^0\left( {{C_2}{H_5}OH} \right){\rm{ }} - {\Delta _r}H_{298}^0\left( {{C_2}{H_4}} \right){\rm{ }} - {\Delta _r}H_{298}^0\left( {{H_2}O} \right)\]
C. \[{\Delta _r}H_{298}^0 = {\Delta _f}H_{298}^0\left( {{C_2}{H_5}OH} \right){\rm{ }} - {\Delta _f}H_{298}^0\left( {{C_2}{H_4}} \right){\rm{ }} - {\Delta _f}H_{298}^0\left( {{H_2}O} \right)\]
D. \[{\Delta _r}H_{298}^0 = {\rm{ }}{\Delta _f}H_{298}^0\left( {{C_2}{H_4}} \right){\rm{ + }}{\Delta _f}H_{298}^0\left( {{H_2}O} \right) - {\Delta _f}H_{298}^0\left( {{C_2}{H_5}OH} \right)\]
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Xem tiếp với tài khoản VIP
Còn 6/12 câu hỏi, đáp án và lời giải chi tiết.
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















