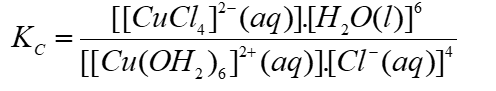Nước có lượng đáng kể các cation Al3+ và Fe3+ được gọi là nước nhiễm phèn. Trong nước nhiễm phèn, mỗi cation này bị thuỷ phân tạo thành phức chất gồm 1 nguyên tử trung tâm, 3 phối tử OH- và 3 phối từ H2O.
a) Viết phương trình hoá học của các phản ứng diễn ra.
b) Vì sao nước phèn có pH thấp?
c) Vì sao trong nước phèn xuất hiện các chất lơ lửng không tan?
Nước có lượng đáng kể các cation Al3+ và Fe3+ được gọi là nước nhiễm phèn. Trong nước nhiễm phèn, mỗi cation này bị thuỷ phân tạo thành phức chất gồm 1 nguyên tử trung tâm, 3 phối tử OH- và 3 phối từ H2O.
a) Viết phương trình hoá học của các phản ứng diễn ra.
b) Vì sao nước phèn có pH thấp?
c) Vì sao trong nước phèn xuất hiện các chất lơ lửng không tan?
Quảng cáo
Trả lời:
a) Phương trình hóa học:
Al3+(aq) + 6H2O(l) → [Al(OH2)6]3+(aq);
[Al(OH2)6]3+(aq) [Al(OH)3(OH2)3](s) + 3H+(aq)
Fe3+(aq) + 6H2O(l) → [Fe(OH2)6]3+(aq);
[Fe(OH2)6]3+(aq) [Fe(OH)3(OH2)3](s) + 3H+(aq)
b) Vì các phản ứng tạo phức xảy ra hình thành H+ tạo môi trường acid → pH thấp.
c) Đó là các sản phẩm phức [Al(OH)3(OH2)3] và [Fe(OH)3(OH2)3]. Phức chất này có dạng keo nên kết dính phù sa, cặn bã … trong nước.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
Có hai thí nghiệm dưới đây.
Thí nghiệm 1 ở 0°C: Có một ống nghiệm chứa 1 mL dung dịch copper(II) sulfate 0,5% màu xanh nhạt. Thêm từ từ cho đến hết 2 mL dung dịch hydrochloric acid đặc không màu vào ống nghiệm đó thì thu được dung dịch có màu vàng chanh do có quá trình:
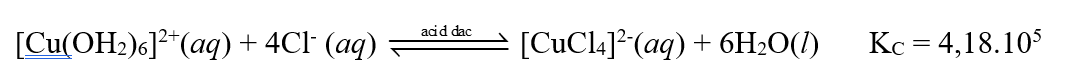
Thí nghiệm 2 ở 20°C: Có một ống nghiệm chứa 1 mL dung dịch copper(II) sulfate 0,5% màu xanh nhạt. Thêm từ từ cho đến hết 2 mL dung dịch sodium chloride bão hoà không màu vào ống nghiệm đó thì thu được dung dịch có màu xanh nhạt hơn so với ban đầu.
Mỗi phát biểu sau đây đúng hay sai?
(a) Biểu thức tính hằng số cân bằng của phản ứng ở thí nghiệm 1 là:
Có hai thí nghiệm dưới đây.
Thí nghiệm 1 ở 0°C: Có một ống nghiệm chứa 1 mL dung dịch copper(II) sulfate 0,5% màu xanh nhạt. Thêm từ từ cho đến hết 2 mL dung dịch hydrochloric acid đặc không màu vào ống nghiệm đó thì thu được dung dịch có màu vàng chanh do có quá trình:
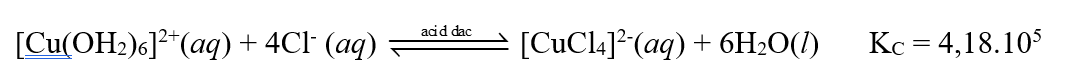
Thí nghiệm 2 ở 20°C: Có một ống nghiệm chứa 1 mL dung dịch copper(II) sulfate 0,5% màu xanh nhạt. Thêm từ từ cho đến hết 2 mL dung dịch sodium chloride bão hoà không màu vào ống nghiệm đó thì thu được dung dịch có màu xanh nhạt hơn so với ban đầu.
Mỗi phát biểu sau đây đúng hay sai?
(a) Biểu thức tính hằng số cân bằng của phản ứng ở thí nghiệm 1 là:
Lời giải
(a) Đúng.
(b) Sai. Phản ứng thuận K lớn hơn nên thuận lợi hơn.
(c) Đúng.
(d) Đúng. Nếu hình thành phức [CuCl4]2-(aq) phải có màu vàng chanh nhưng thí nghiệm 2 không thấy hiện tượng này
Câu 2
Khi cho dung dịch ammonia dư vào dung dịch chứa phức chất [Ni(OH2)6]2+ và anion Cl- thì có phản ứng sau:
[Ni(OH2)6]2+(aq) + 6NH3(aq) → [Ni(NH3)6]2+(aq) + 6H2O(l) (*)
Phát biểu nào dưới đây là không đúng?
A. Trong điều kiện của phản ứng (*), phức chất [Ni(NH3)6]2+(aq) kém bền hơn phức chất [Ni(OH2)6]2+(aq).
B. Phản ứng (*) là phản ứng thế phối tử.
C. Dung dịch sau phản ứng có pH > 7.
D. Trong phản ứng không có sự thay đôi số oxi hoá của các nguyên tố.
Khi cho dung dịch ammonia dư vào dung dịch chứa phức chất [Ni(OH2)6]2+ và anion Cl- thì có phản ứng sau:
[Ni(OH2)6]2+(aq) + 6NH3(aq) → [Ni(NH3)6]2+(aq) + 6H2O(l) (*)
Phát biểu nào dưới đây là không đúng?
A. Trong điều kiện của phản ứng (*), phức chất [Ni(NH3)6]2+(aq) kém bền hơn phức chất [Ni(OH2)6]2+(aq).
B. Phản ứng (*) là phản ứng thế phối tử.
C. Dung dịch sau phản ứng có pH > 7.
D. Trong phản ứng không có sự thay đôi số oxi hoá của các nguyên tố.
Lời giải
Đáp án đúng là: A
Trong điều kiện của phản ứng (*), phức chất [Ni(NH3)6]2+(aq) bền hơn phức chất [Ni(OH2)6]2+(aq).
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
Khi hoà tan một lượng phèn nhôm - kali vào nước thì có các quá trình cơ bản sau diễn ra:
Al3+(aq) + 6H2O(l) → [Al(OH2)6]3+(aq) (1)
[Al(OH2)6]3+(aq) + 3H2O(l) [Al(OH)3(H2O)3](s) + 3H3O+(aq) (2)
Mỗi phát biểu sau đây là đúng hay sai?
(a) Quá trình (1) là quá trình tạo phức chất aqua của cation Al3+. Quá trình này diễn ra rất thuận lợi.
(b) Các quá trình (1) và (2) giúp giải thích vì sao cation Al3+ là một base trong dung dịch nước theo Bronsted – Lowry.
(c) Ở quá trình (2), các phân tử nước đóng vai trò là dung môi.
(d) Để thu được nhiều kết tủa keo thì cần hoà tan lượng nhỏ phèn trong lượng lớn nước.
Khi hoà tan một lượng phèn nhôm - kali vào nước thì có các quá trình cơ bản sau diễn ra:
Al3+(aq) + 6H2O(l) → [Al(OH2)6]3+(aq) (1)
[Al(OH2)6]3+(aq) + 3H2O(l) [Al(OH)3(H2O)3](s) + 3H3O+(aq) (2)
Mỗi phát biểu sau đây là đúng hay sai?
(a) Quá trình (1) là quá trình tạo phức chất aqua của cation Al3+. Quá trình này diễn ra rất thuận lợi.
(b) Các quá trình (1) và (2) giúp giải thích vì sao cation Al3+ là một base trong dung dịch nước theo Bronsted – Lowry.
(c) Ở quá trình (2), các phân tử nước đóng vai trò là dung môi.
(d) Để thu được nhiều kết tủa keo thì cần hoà tan lượng nhỏ phèn trong lượng lớn nước.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
Cho các quá trình tạo phức chất bát diện sau:
![Cho các quá trình tạo phức chất bát diện sau: Biết dung dịch [Fe(OH2)6]3+ màu vàng nâu, dung dịch [Fe(OH2)5(SCN)]2+ có màu đỏ, dung dịch [Fe(OH2)5F]2+ và các anion SCN-, F- đều không có màu. (ảnh 1)](https://video.vietjack.com/upload2/quiz_source1/2024/08/blobid4-1724945356.png)
Biết dung dịch [Fe(OH2)6]3+ màu vàng nâu, dung dịch [Fe(OH2)5(SCN)]2+ có màu đỏ, dung dịch [Fe(OH2)5F]2+ và các anion SCN-, F- đều không có màu.
Mỗi phát biểu sau đây đúng hay sai?
(a) Quá trình (I) xảy ra khi hoà tan iron(III) chloride trong nước. Kết thúc quá trình này thu được dung dịch có chứa lượng lớn cation Fe3+ và phức chất aqua [Fe(OH2)6]3+.
(b) So với anion F-, anion SCN- dễ thay thế phối tử H2O trong [Fe(OH)6]3+ hơn.
(c) Khi cho từ từ dung dịch KSCN vào dung dịch ở quá trình (III) thì dung dịch này sẽ có màu.
(d) Trong các quá trình (I), (II) và (III), mỗi phân tử H2O hoặc anion SCN- hay anion F- đều sử dụng số cặp electron hoá trị riêng như nhau để cho vào orbital trống của cation Fe3+.
Cho các quá trình tạo phức chất bát diện sau:
![Cho các quá trình tạo phức chất bát diện sau: Biết dung dịch [Fe(OH2)6]3+ màu vàng nâu, dung dịch [Fe(OH2)5(SCN)]2+ có màu đỏ, dung dịch [Fe(OH2)5F]2+ và các anion SCN-, F- đều không có màu. (ảnh 1)](https://video.vietjack.com/upload2/quiz_source1/2024/08/blobid4-1724945356.png)
Biết dung dịch [Fe(OH2)6]3+ màu vàng nâu, dung dịch [Fe(OH2)5(SCN)]2+ có màu đỏ, dung dịch [Fe(OH2)5F]2+ và các anion SCN-, F- đều không có màu.
Mỗi phát biểu sau đây đúng hay sai?
(a) Quá trình (I) xảy ra khi hoà tan iron(III) chloride trong nước. Kết thúc quá trình này thu được dung dịch có chứa lượng lớn cation Fe3+ và phức chất aqua [Fe(OH2)6]3+.
(b) So với anion F-, anion SCN- dễ thay thế phối tử H2O trong [Fe(OH)6]3+ hơn.
(c) Khi cho từ từ dung dịch KSCN vào dung dịch ở quá trình (III) thì dung dịch này sẽ có màu.
(d) Trong các quá trình (I), (II) và (III), mỗi phân tử H2O hoặc anion SCN- hay anion F- đều sử dụng số cặp electron hoá trị riêng như nhau để cho vào orbital trống của cation Fe3+.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
Mỗi phát biểu dưới đây đúng hay sai?
(a) Trong nước, cation của kim loại M (có hoá trị n) thường tồn tại ở dạng phức chất aqua [M(OH2)m]n+.
(b) Các phức chất aqua [M(OH2)m]n+ luôn có màu.
(c) Trong nhiều phức chất aqua [M(OH2)m]n+, số phối tử thường là 6.
(d) Phức chất aqua [M(OH2)m]n+ có thể tan hoặc không tan trong nước.
Mỗi phát biểu dưới đây đúng hay sai?
(a) Trong nước, cation của kim loại M (có hoá trị n) thường tồn tại ở dạng phức chất aqua [M(OH2)m]n+.
(b) Các phức chất aqua [M(OH2)m]n+ luôn có màu.
(c) Trong nhiều phức chất aqua [M(OH2)m]n+, số phối tử thường là 6.
(d) Phức chất aqua [M(OH2)m]n+ có thể tan hoặc không tan trong nước.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
Khi hòa tan zinc(II)chloride trong nước, diễn ra một số quá trình cơ bản sau:
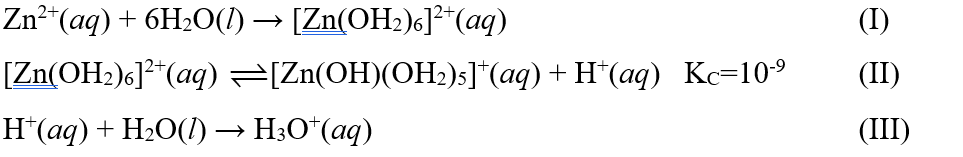
Cho các phát biểu sau:
(1) Quá trình (I) và (III) có thể diễn ra yếu hơn quá trình (II).
(2) Từ quá trình (II) có thể suy ra “[Zn(OH2)6]2+ là acid theo Arrhenius”.
(3) Từ quá trình (III) có thể suy ra “H2O là base theo Bronsted - Lowry”.
(4) Từ quá trình (I), (II) và (III) suy ra “trong nước, cation Zn2+ là acid theo Bronsted - Lowry”.
(5) Dung dịch zinc(II) chloride có tính acid khá mạnh.
(6) Trong dung dịch zinc(II) chloride, nước vừa là dung môi, vừa đóng vai trò base theo Bronsted - Lowry.
Số phát biểu đúng là:
A. 2. B. 3. C. 4. D 5
Khi hòa tan zinc(II)chloride trong nước, diễn ra một số quá trình cơ bản sau:
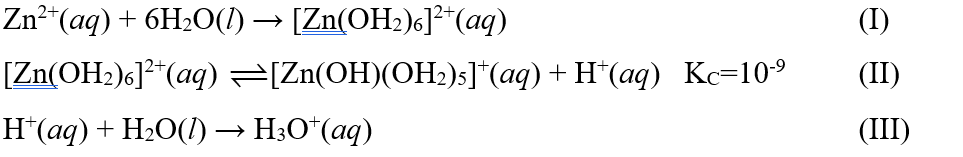
Cho các phát biểu sau:
(1) Quá trình (I) và (III) có thể diễn ra yếu hơn quá trình (II).
(2) Từ quá trình (II) có thể suy ra “[Zn(OH2)6]2+ là acid theo Arrhenius”.
(3) Từ quá trình (III) có thể suy ra “H2O là base theo Bronsted - Lowry”.
(4) Từ quá trình (I), (II) và (III) suy ra “trong nước, cation Zn2+ là acid theo Bronsted - Lowry”.
(5) Dung dịch zinc(II) chloride có tính acid khá mạnh.
(6) Trong dung dịch zinc(II) chloride, nước vừa là dung môi, vừa đóng vai trò base theo Bronsted - Lowry.
Số phát biểu đúng là:
A. 2. B. 3. C. 4. D 5
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.