Kết quả phân tích nguyên tố của hợp chất amine thơm X có phần trăm khối lượng các nguyên tố như sau: %C = 78,51%; %H = 8,41%; %N = 13,08%. Từ phổ khối lượng (MS) xác định được phân tử khối của X bằng 107. Ứng với công thức phân tử của X, có bao nhiêu amine thơm, kể cả X?
Câu hỏi trong đề: Đề kiểm tra Hóa 12 Kết nối tri thức Chương 3 có đáp án !!
Quảng cáo
Trả lời:
Hướng dẫn giải
Đáp án đúng là: C
Gọi công thức phân tử của amine thơm X có dạng \({C_x}{H_y}{N_z}.\)
Ta có: \(\frac{{{M_X}}}{{100\% }} = \frac{{12x}}{{\% C}} = \frac{y}{{\% H}} = \frac{{14z}}{{\% N}}\)
⇒ \(x = \frac{{107.78,51}}{{12.100}} = 7;y = \frac{{107.8,41}}{{100}} = 9;z = \frac{{107.13,08}}{{14.100}} = 1\)
⇒ Công thức phân tử của amine thơm X là \({C_7}{H_9}N.\)
Các đồng phân thỏa mãn là: \(\,{H_2}N - {C_6}{H_4} - C{H_3}(o,p,m);\,{C_6}{H_5} - NH - C{H_3}.\)
⇒ Tổng có 4 đồng phân amine thơm.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Hướng dẫn giải
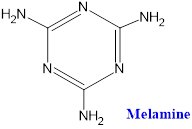
a. Đúng. Một phân tử melamine công thức phân tử là C3H6N6 nên có công thức đơn giản nhất là CH2N2 và có 9 liên kết (trên công thức cấu tạo) + 6 nguyên tử H = 15 liên kết sigma (σ).
b. Đúng.
c. Sai. Melamine có tính base nhưng không thuộc loại arylamine.
d. Đúng. Muốn tăng 1 độ đạm (1 g nitrogen) cho sữa tươi thì phải thêm vào 1 lít sữa khoảng 1,5g hay 1500 mg melamine (tức là 1500ppm).
Tính bằng cách:
Cứ melanine (C3H6N6) có phân tử khối bằng 126 gam, chứa 6 nitrogen tức 6.14 = 84 gam.
Vậy để có 1 độ đạm tương ứng 1 gam nitrogen cần:
\[\frac{{1.126}}{{84}} = {\rm{ }}1,5{\rm{ }}gam = 1500{\rm{ }}mg{\rm{ }}melamine\].
Câu 2
Lời giải
Hướng dẫn giải
Đáp án đúng là: D
Ethylmethylamine: CH3CH2NHCH3 là amine bậc hai, do có 2 H trong NH3 bị thay thế bởi gốc hydrocarbon.
Câu 3
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.