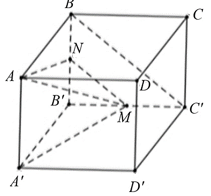
Cho hình lập phương \(ABCD.A'B'C'D'.\) Gọi \(M\) là trung điểm của \(B'C'.\) Góc giữa hai đường thẳng AM và \(BC'\) bằng
Cho hình lập phương \(ABCD.A'B'C'D'.\) Gọi \(M\) là trung điểm của \(B'C'.\) Góc giữa hai đường thẳng AM và \(BC'\) bằng
Quảng cáo
Trả lời:
Giả sử cạnh của hình lập phương là \(a > 0.\)
Gọi \(N\) là trung điểm đoạn thẳng \(BB'.\)
Khi đó, \(MN\,{\rm{//}}\,BC'\) nên \(\left( {AM\,,\,\,BC'} \right) = \left( {AM\,,\,MN} \right)\).
Xét \(\Delta A'B'M\) vuông tại \(B'\), ta có
\(A'M = \sqrt {A'{{B'}^{\prime 2}} + B'{M^2}} = \sqrt {{a^2} + \frac{{{a^2}}}{4}} = \frac{{a\sqrt 5 }}{2}.\)
Xét \(\Delta AA'M\) vuông tại \(A'\), ta có \(AM = \sqrt {A{{A'}^2} + A'{M^2}} = \sqrt {{a^2} + \frac{{5{a^2}}}{4}} = \frac{{3a}}{2}.\)
Có \[AN = A'M = \frac{{a\sqrt 5 }}{2}\,;\,\,MN = \frac{{BC'}}{2} = \frac{{a\sqrt 2 }}{2}.\]
Trong tam giác \[AMN\] ta có: \(\cos \widehat {AMN} = \frac{{M{A^2} + M{N^2} - A{N^2}}}{{2MA \cdot MN}} = \frac{{\frac{{9{a^2}}}{4} + \frac{{2{a^2}}}{4} - \frac{{5{a^2}}}{4}}}{{2 \cdot \frac{{3a}}{2} \cdot \frac{{a\sqrt 2 }}{2}}} = \frac{1}{{\sqrt 2 }}.\)
Suy ra \(\widehat {AMN} = 45^\circ .\) Vậy \[\left( {AM,\,\,BC'} \right) = \left( {AM,\,\,MN} \right) = \widehat {AMN} = 45^\circ .\] Chọn A.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
Khi thêm 1,0 gam \(MgS{O_4}\) khan vào 100 gam dung dịch \(MgS{O_4}\) bão hòa ở \({20^o}C\) đã làm tách ra 1,58 gam \(MgS{O_4}\) kết tinh dưới dạng \(MgS{O_4}.n{H_2}O.\) Biết độ tan của \(MgS{O_4}\) ở \({20^o}C\) là 35,1 gam. Công thức của muối kết tinh tách ra là
Lời giải
- Ở \({20^o}C\), độ tan của \(MgS{O_4}\) là 35,1 gam nên khối lượng \(MgS{O_4}\)có trong 100 gam dung dịch \(MgS{O_4}\) bão hòa là: \({m_{MgS{O_4}}} = \frac{{100.35,1}}{{(100 + 35,1)}} = 25,98\,gam\)
Sau khi thêm 1,0 gam \(MgS{O_4}\) vào 100 gam dung dịch bão hòa thì khối lượng \(MgS{O_4}\) còn lại trong dung dịch là: 1,0 + 25,98 – 1,58 = 25,4 gam.
- Nồng độ bão hòa dung dịch \(MgS{O_4}\) ở \({20^o}C\) là \(C\% = \frac{{25,98}}{{100}}.100 = 25,98\% \)
- Số mol \(MgS{O_4}\) bằng với số mol tinh thể tách ra \(MgS{O_4}.n{H_2}O\) bằng \(\frac{{1,58}}{{120}}\) mol
- Khối lượng dung dịch sau khi tinh thể tách ra là:
\({m_{dd}} = 1 + 100 - 1,58 - \frac{{1,58}}{{120}}.18n = 99,42 - 0,237n\,(g)\)
→ \(\frac{{25,4}}{{99,42 - 0,237n}}.100 = 25,98\) → n = 7.
→ Công thức muối kết tinh tách ra là: \(MgS{O_4}.7{H_2}O.\)
Chọn C.
Lời giải
Đáp án đúng là A
Theo định luật bảo toàn: tổng số nuclôn của các hạt tương tác bằng tổng số nuclôn của các hạt sản phẩm: \({A_n} + {A_U} = {A_{Zr}} + {A_{Ce}} + x \cdot {A_n} + y \cdot {A_e} \to 1 + 235 = 92 + 142 + x.1 + y \cdot 0 \to x = 2\)
Tổng đại số các điện tích của các hạt tương tác bằng tổng đại số các điện tích của các hạt sản phẩm: \({Z_n} + {Z_U} = {Z_{Zr}} + {Z_{Ce}} + x \cdot {Z_n} + y.{Z_e} \to 0 + 92 = 40 + 58 + x.0 + y.( - 1) \to y = 6\)
Câu 3
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















