Biến thiên enthalpy chuẩn của một phản ứng hoá học là nhiệt lượng toả ra hay thu vào của một phản ứng hóa học ở điều kiện chuẩn (áp suất 1 bar, nhiệt độ 25oC và nồng độ dung dịch là 1 M), được kí hiệu là \[{{\rm{\Delta }}_r}H_{298}^o\]. Phản ứng tỏa nhiệt là phản ứng hóa học khi xảy ra sẽ giải phóng nhiệt lượng ra môi trường và \[{{\rm{\Delta }}_r}H < 0\]. Trong khi ngược lại, phản ứng thu nhiệt là phản ứng hóa học cần sự hấp thụ nhiệt từ môi trường và \[{{\rm{\Delta }}_r}H > 0\].
Có thể dự đoán sơ bộ chiều hướng xảy ra của một phản ứng hóa học thông qua tính toán giá trị biến thiên enthalpy chuẩn của phản ứng đó. Việc tính toán giá trị biến thiên enthalpy của một phản ứng có thể được thực hiện tính toán thông qua nhiệt tạo thành chuẩn của chất tham gia và chất sản phẩm:
\[{{\rm{\Delta }}_r}H_{298}^o = {\rm{\Sigma }}{{\rm{\Delta }}_f}H_{298}^o(sp) - {\rm{\Sigma }}{{\rm{\Delta }}_f}H_{298}^o(cd)\]
Trong đó \[{{\rm{\Delta }}_f}H_{298}^o\] là nhiệt tạo thành chuẩn (kJ/mol). Biểu thức trên có thể phát biểu: Biến thiên enthalpy chuẩn của một phản ứng hóa học bằng tổng nhiệt tạo thành chuẩn của chất sản phẩm trừ tổng nhiệt tạo thành chuẩn của chất đầu tham gia phản ứng.
Một công ty đang phát triển sản phẩm “túi sưởi khẩn cấp” sử dụng phản ứng hóa học để làm ấm cơ thể trong mùa đông. Bên trong túi sưởi chứa hỗn hợp CaCl2 khan và một lượng nước nhỏ trong ngăn kín. Khi bóp vỡ ngăn chứa nước, nước sẽ trộn với CaCl2 tạo thành dung dịch CaCl2(aq) kèm theo tỏa nhiệt giúp cung cấp nhiệt tức thời cho người dùng.
Phản ứng: CaCl2(s) → CaCl2(aq)
Công ty muốn thiết kế sản phẩm sao cho khi hòa tan m gam CaCl2 vào 250 mL nước (d = 1,0 g/mL), nước sẽ nóng lên từ 5°C đến 25°C để đảm bảo hiệu quả làm ấm.
Biết:
- Nhiệt dung riêng (năng lượng cần để tăng nhiệt độ của 1g chất lên 10C) của nước là 4,18 J/g.K.
- Hiệu suất truyền nhiệt của túi sưởi là 85%.
- Nhiệt tạo thành tiêu chuẩn (kJ/mol) của các chất liên quan như sau:
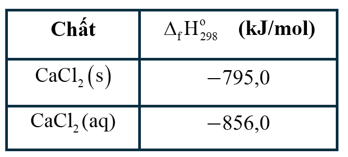
Quá trình hoà tan CaCl2(s) vào nước thuộc loại quá trình nào sau đây?
Biến thiên enthalpy chuẩn của một phản ứng hoá học là nhiệt lượng toả ra hay thu vào của một phản ứng hóa học ở điều kiện chuẩn (áp suất 1 bar, nhiệt độ 25oC và nồng độ dung dịch là 1 M), được kí hiệu là \[{{\rm{\Delta }}_r}H_{298}^o\]. Phản ứng tỏa nhiệt là phản ứng hóa học khi xảy ra sẽ giải phóng nhiệt lượng ra môi trường và \[{{\rm{\Delta }}_r}H < 0\]. Trong khi ngược lại, phản ứng thu nhiệt là phản ứng hóa học cần sự hấp thụ nhiệt từ môi trường và \[{{\rm{\Delta }}_r}H > 0\].
Có thể dự đoán sơ bộ chiều hướng xảy ra của một phản ứng hóa học thông qua tính toán giá trị biến thiên enthalpy chuẩn của phản ứng đó. Việc tính toán giá trị biến thiên enthalpy của một phản ứng có thể được thực hiện tính toán thông qua nhiệt tạo thành chuẩn của chất tham gia và chất sản phẩm:
\[{{\rm{\Delta }}_r}H_{298}^o = {\rm{\Sigma }}{{\rm{\Delta }}_f}H_{298}^o(sp) - {\rm{\Sigma }}{{\rm{\Delta }}_f}H_{298}^o(cd)\]
Trong đó \[{{\rm{\Delta }}_f}H_{298}^o\] là nhiệt tạo thành chuẩn (kJ/mol). Biểu thức trên có thể phát biểu: Biến thiên enthalpy chuẩn của một phản ứng hóa học bằng tổng nhiệt tạo thành chuẩn của chất sản phẩm trừ tổng nhiệt tạo thành chuẩn của chất đầu tham gia phản ứng.
Một công ty đang phát triển sản phẩm “túi sưởi khẩn cấp” sử dụng phản ứng hóa học để làm ấm cơ thể trong mùa đông. Bên trong túi sưởi chứa hỗn hợp CaCl2 khan và một lượng nước nhỏ trong ngăn kín. Khi bóp vỡ ngăn chứa nước, nước sẽ trộn với CaCl2 tạo thành dung dịch CaCl2(aq) kèm theo tỏa nhiệt giúp cung cấp nhiệt tức thời cho người dùng.
Phản ứng: CaCl2(s) → CaCl2(aq)
Công ty muốn thiết kế sản phẩm sao cho khi hòa tan m gam CaCl2 vào 250 mL nước (d = 1,0 g/mL), nước sẽ nóng lên từ 5°C đến 25°C để đảm bảo hiệu quả làm ấm.
Biết:
- Nhiệt dung riêng (năng lượng cần để tăng nhiệt độ của 1g chất lên 10C) của nước là 4,18 J/g.K.
- Hiệu suất truyền nhiệt của túi sưởi là 85%.
- Nhiệt tạo thành tiêu chuẩn (kJ/mol) của các chất liên quan như sau:

Quá trình hoà tan CaCl2(s) vào nước thuộc loại quá trình nào sau đây?
Quảng cáo
Trả lời:
Đáp án đúng là B
Phương pháp giải
Dựa vào hiện tượng của mà túi sưởi mang lại.
Lời giải
Do túi sưởi cung cấp nhiệt được chứng tỏ có sự tỏa nhiệt từ phản từ phản ứng chuyển hóa CaCl2(s) → CaCl2(aq).
Vậy quá trình hoà tan CaCl2(s) vào nước thuộc loại phản ứng tỏa nhiệt.
Câu hỏi cùng đoạn
Câu 2:
Nhiệt lượng cần cung cấp để làm nóng 250 mL nước (d = 1,0 g/mL) từ 5°C lên 25°C là
Nhiệt lượng cần cung cấp để làm nóng 250 mL nước (d = 1,0 g/mL) từ 5°C lên 25°C là
Đáp án đúng là B
Phương pháp giải
Tính khối lượng nước, tính độ thay đổi nhiệt độ, từ đó tính nhiệt lượng cần.
Lời giải
Khối lượng nước: m = V.D = 250g
Nhiệt lượng cần cung cấp để 250g nước tăng 20oC là: 250.4,18.20 = 20,9J.
Câu 3:
Nếu hiệu suất truyền nhiệt của túi sưởi là 85%, nhiệt lượng cần sinh ra từ phản ứng hòa tan CaCl2(s)
Đáp án đúng là B
Phương pháp giải
Tính lượng nhiệt thực tế cần cung cấp dựa theo hiệu suất truyền nhiệt.
Lời giải
Hiệu suất truyền nhiệt 85% nên nhiệt lượng thực tế cần: 20,9 : 85% = 24,588J.
Chọn đáp án B.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án đúng là A
Phương pháp giải
- Tính khối lượng tinh bột thực tế mà người đó tiêu thụ.
- Tinh bột bị thủy phân thành glucose.
- Glucose bị thủy phân chuyển hóa thành năng lượng.
Lời giải
- Số mol tinh bột trong gạo: \[\frac{{64,8.80{\rm{\% }}}}{{162}} = 0,32mol\]
Phản ứng thủy phân tinh bột: \[{n_{{C_6}{H_{12}}{O_6}}} = {n_{{C_6}{H_{12}}{O_6}}} = 0,32mol\]
- Lượng nhiệt dư thừa của 1 ngày: \[0,32.2800 = 896kJ\].
- Lượng nhiệt dư thừa của 30 ngày: \[896.30 = 26880kJ\].
- Khối lượng mỡ tích được trong cơ thể người: \[\frac{{26880}}{{40}} = 672g\]
Câu 2
Lời giải
Đáp án đúng là C
Phương pháp giải
- Tính lượng nhiệt cần cung cấp để tạo ra 42 tấn vôi sống CaO (1).
- Tính lượng nhiệt do 84% của 10 tấn than đá đã cung cấp (2).
- Lấy kết quả (1)/(2) để tính hiệu suất hấp thụ nhiệt.
Lời giải
- Lượng nhiệt cần cung cấp để tạo ra 42 tấn vôi sống CaO là: \[{Q_1} = \frac{{{{42.10}^6}}}{{56}}.180 = {135.10^6}kJ\]
- Lượng nhiệt do đốt cháy 10 tấn than đá là: \[{Q_2} = \frac{{{{10.10}^6}.84{\rm{\% }}}}{{12}}.390 = {273.10^6}kJ\].
- Hiệu suất hấp thụ nhiệt của quá trình phân hủy đá vôi là: \[H = \frac{{{Q_1}}}{{{Q_2}}}.100{\rm{\% }} = \frac{{{{135.10}^6}}}{{{{273.10}^6}}}.10{\rm{\% }} \approx 49,5{\rm{\% }}\]
Chọn đáp án C.
Câu 3
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
B. Các loài côn trùng nhỏ có khả năng phân hủy chất hữu cơ và tái chế chất dinh dưỡng.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















